(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示______,K值大小与温度的关系是:温度升高,K值______ (填一定增大、一定减小、或可能增大也可能减小).
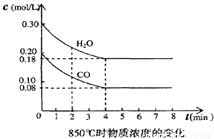
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如下图所示,则0~4min的平均反应速率v(CO)=______mol/
t1℃时物质浓度(mol/L)的变化
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min~4min之间反应处于______状态;C1数值______0.08mol/L (填大于、小于或等于).
②反应在4min~5min之间,平衡向逆方向移动,可能的原因是______ (单选),表中5min~6min之间数值发生变化,可能的原因是______ (单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
0 62398 62406 62412 62416 62422 62424 62428 62434 62436 62442 62448 62452 62454 62458 62464 62466 62472 62476 62478 62482 62484 62488 62490 62492 62493 62494 62496 62497 62498 62500 62502 62506 62508 62512 62514 62518 62524 62526 62532 62536 62538 62542 62548 62554 62556 62562 62566 62568 62574 62578 62584 62592 203614
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O浓度变化如下图所示,则0~4min的平均反应速率v(CO)=______mol/
t1℃时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0.200 | 0.300 | |||
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.006 | 0.266 | 0.104 |
①表中3min~4min之间反应处于______状态;C1数值______0.08mol/L (填大于、小于或等于).
②反应在4min~5min之间,平衡向逆方向移动,可能的原因是______ (单选),表中5min~6min之间数值发生变化,可能的原因是______ (单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
