垃圾焚烧发电产生的烟气中含烟尘、二氧化硫、氮氧化物、氯化氢等有害物质,某处理流程如下:
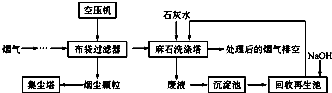
(1)麻石洗涤塔中设置多层格栅,上面放置大量耐酸碱塑料小球,塔内设置多层上喷下淋水嘴,“烟气”从塔底进入,目的是______.
(2)若NO2和NO气体以物质的量之比1:1混合通入石灰水中,发生氧化还原反应生成一种正盐和水,请写出该反应的化学方程式:______;已知此正盐的水溶液呈碱性,用离子方程式表示为______.
(3)废液在沉淀池中慢慢沉降,沉淀主要含______;在回收再生池中加入NaOH固体的作用是______.
(4)环境检测部门测量处理前后烟气中烟尘的含量见下表:
| 项目 | 监测结果 | 国标号 | |
| 处理前 | 处理后 | GWKB3-2 000 | |
| 烟尘(mg?m-3) | 13 929.0 | 61.0 | 80 |

