下列说法正确的是( )
| A、一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H>0、△S<0 | ||
B、水解反应NH
| ||
| C、铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | ||
| D、为了降低水库的铁闸门被腐蚀的速率,焊接在铁闸门上的固体材料可以采用金属锌 |
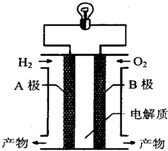 氢氧燃料电池是一种新能源.如图为氢氧燃料电池示意图.下列说法不正确的是( )
氢氧燃料电池是一种新能源.如图为氢氧燃料电池示意图.下列说法不正确的是( )| A、该装置能将化学能转化为电能 | B、A极是正极,B极是负极 | C、电子由A极通过导线流向B极 | D、产物为无污染的水,属于环境友好电池 |
心脏起搏器中使用的是Li-I2可充电电池,使用寿命约10年.下列说法中正确的是( )
| A、因为LiI在水中的溶解度比在有机溶剂中大,所以选用水溶液做电解质 | |||
B、电池反应方程式为2Li+I2
| |||
| C、电池的负极为I2 | |||
| D、充电时,阳极反应为2LiI→Li+2I-+2e- |
 某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示(上端为多孔电极a,下断为多孔电极b),该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法不正确的是( )
某汽车尾气分析仪以燃料电池为工作原理测定CO的浓度,其装置如图所示(上端为多孔电极a,下断为多孔电极b),该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法不正确的是( )| A、工作时电极b作正极,O2-由电极b流向电极a | B、工作时电子由电极a通过介质流向电极b | C、负极的电极反应式为:CO+O2--2e-=CO2 | D、传感器中通过的电流越大,尾气中CO的含量越高 |
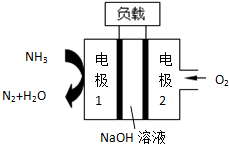 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图,有关说法正确的是( )| A、电池工作时,Na+向负极移动 | B、电子由电极2经外电路流向电极1 | C、电池总反应为:4NH3+3O2=2N2+6H2O | D、电极2发生的电极反应为:O2+4H ++4e-=2H2O |
 二甲醚是一种绿色、可再生的新能源.如图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )
二甲醚是一种绿色、可再生的新能源.如图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法不正确的是( )| A、a电极为该电池负极 | B、O2在b电极上得电子,被氧化 | C、电池工作时,a电极反应式:CH3OCH3-12e-+3H2O→2CO2↑+12H+ | D、电池工作时,燃料电池内部H+从a电极移向b电极 |
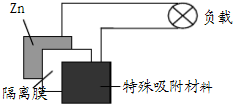 锌-空气电池因其安全、廉价而且能量密度高,科学家预测可充电锌-空气电池将引领电池革命.这种电池使用特殊材料吸附空气中的氧气,以强碱溶液为电解质.该电池放电时的总反应为2Zn+O2=2ZnO.下列判断正确的是( )
锌-空气电池因其安全、廉价而且能量密度高,科学家预测可充电锌-空气电池将引领电池革命.这种电池使用特殊材料吸附空气中的氧气,以强碱溶液为电解质.该电池放电时的总反应为2Zn+O2=2ZnO.下列判断正确的是( )| A、放电时锌作电池的正极,发生氧化反应 | B、放电时,正极反应式:Zn+2 OH--2e-=ZnO+H2O | C、充电时,阴极反应式:O2+2H2O+4e-=4 OH- | D、电池中的隔离膜只允许OH-通过 |
优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为:2Li+P2VP?nI2=P2VP?(n-1)I2+2LiI,则下列说法正确的( )
| A、该电池的电势低,使用寿命比较短 | B、电池工作时,碘离子移向P2VP一极 | C、聚2-乙烯吡啶的复合物与有机物性质相似,因此不会导电 | D、正极的反应为:P2VP?nI2+2Li++2e-=P2VP?(n-1)I2+2LiI |
铅蓄电池是典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-?2PbSO4+2H2O.下列说法正确的是( )
| A、放电时,负极的电极反应式是PbO2+4H++SO42-+2e-=PbSO4+2H2O | B、充电时,电解液中H2SO4的浓度将变小 | C、放电时,PbO2发生氧化反应 | D、充电时,蓄电池的正极和外接电源的正极相连 |
10℃时,在烧杯中加入0.1mol/L的NaHCO3溶液400mL,加热,测得该溶液的PH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为: ;
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度 (填“大于”或“小于”)NaHCO3;
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH 8.3(填“>”、“<”或“=”),说明乙正确;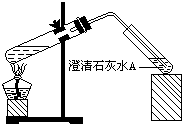
(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明 (填“甲”或“乙”)推断正确;
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断 (填“甲”或“乙”)推测正确,原因是 .
0 60619 60627 60633 60637 60643 60645 60649 60655 60657 60663 60669 60673 60675 60679 60685 60687 60693 60697 60699 60703 60705 60709 60711 60713 60714 60715 60717 60718 60719 60721 60723 60727 60729 60733 60735 60739 60745 60747 60753 60757 60759 60763 60769 60775 60777 60783 60787 60789 60795 60799 60805 60813 203614
| 温度(℃) | 10 | 20 | 30 | 40 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH

(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明
(5)将一定体积0.1mol/L的NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为10.4;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为9.5.据此资料可以判断