下列溶液一定呈酸性的是( )
| A、pH<7的溶液 | B、c(H+)>c(OH-) 的溶液 | C、pH>7的溶液 | D、c(H+)<c(OH-) 的溶液 |
向纯水中加入少量下列物质或改变下列条件,能促进水的电离,并能使溶液中c(OH-)>c(H+)的操作是( )
①稀硫酸 ②金属钠 ③氨气 ④FeCl3固体 ⑤NaClO固体 ⑥将水加热煮沸.
①稀硫酸 ②金属钠 ③氨气 ④FeCl3固体 ⑤NaClO固体 ⑥将水加热煮沸.
| A、②⑤ | B、①④ | C、③④⑥ | D、④ |
下列措施不能促进水的电离的是( )
| A、升高温度 | B、加入NaHSO4固体 | C、加入金属钠 | D、加入Na2CO3固体 |
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是( )
| A、W2-、X+ | B、Y3+、Z2- | C、X+、Y3+ | D、X+、Z2- |
水的电离平衡为H2O?H+﹢OH-,△H>0,下列叙述不正确的是( )
| A、将水加热,pH减小 | B、恒温下,向水中加入少量固体KOH,Kw不变 | C、向水中滴入稀醋酸,c(H+)增大 | D、向水中加入少量固体NaClO,平衡逆向移动 |
水的电离方程式为H2O?H++OH-,在不同的温度下,其平衡常数K(25℃)=1×10-14,K(35℃)=2.1×10-14,则下列叙述正确的是( )
| A、C(H+)随着温度的升高而降低 | B、在35℃时,c(H+)>c(OH-) | C、水的电离程度α(25℃)>α(35℃) | D、水的电离是吸热的 |
25℃时,水溶液中c(H+)与c(OH-)的变化关系如图中曲线ac所示,下列判断错误的是( )
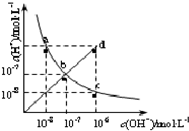

| A、a c曲线上的任意一点都有c(H+)?c(OH-)=10-14 | B、b d线段上任意一点对应的溶液都呈中性 | C、d点对应溶液的温度高于25℃,pH<7 | D、CH3COONa溶液不可能位于c点 |
下列物质溶解于水中,能促进水的电离的是( )
| A、H2SO4 | B、Ba(OH)2 | C、KNO3 | D、Na2CO3 |
下列几种微粒中能影响水的电离平衡,且能使水的电离平衡向右移动的是( )
| A、HSO4- | B、Cl- | C、aX+ 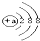 | D、bX2- 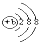 |
常温下,pH=3的H2SO4溶液和pH=11的K2CO3溶液中,水的电离程度( )
| A、H2SO4溶液大 | B、无法确定 | C、一样大 | D、K2CO3溶液大 |