常温下pH为2的盐酸,下列叙述正确的是( )
| A、将10mL该溶液稀释至100mL后,pH小于3 | B、向该溶液中加入等体积pH为12的氨水恰好完全中和 | C、该溶液中由水电离出的c(H+)(水)×c(OH-)(水)═1×10-14 | D、该溶液中盐酸电离的c(H+)与水电离出的c(H+)之比为1010:1 |
下列有关说法正确的是( )
| A、C(s)+CO2(g)=2CO(g)室温下不能自发进行,说明该反应的△H<0 | ||
| B、不锈钢利用牺牲阳极的阴极保护法增强抗腐蚀能力 | ||
C、SO2(g)+2CO(g)
| ||
| D、向水中加入少量固体硫酸氢钠,恢复至原温度,c(H+)增大,Kw不变 |
下列溶液均处于常温下,有关叙述正确的是( )
| A、pH相同的氨水与硫酸等体积混合,所得溶液呈中性 | B、向水中通入氨气,水的电离平衡逆向移动,Kw不变,溶液的c(OH-)增大 | C、向水中加入少量CH3COONa晶体,水的电离平衡正向移动,溶液的c(H+)增大 | D、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的2倍 |
下列条件变化会使H2O的电离平衡向电离方向移动,且pH<7的是( )
| A、将纯水加热到100℃ | B、向水中加少量HCl | C、向水中加少量NaOH | D、向水中加少量Na2CO3 |
下列说法中正确的是( )
A、若温度T℃时水的离子积常数为KW,在该温度下的中性溶液中c(H+)=
| ||||
| B、25℃时HCl溶液中的c(H+) 一定大于25℃时NH4Cl溶液中的C(H+) | ||||
| C、1mol?L-1CH3COOH溶液和1mol?L-1KOH溶液等体积混合,混合溶液中c(K+)=c(CH3COO-) | ||||
D、pH=5.7 的 NaHSO3 溶液中:c(Na+)>c(HSO
|
如图表示水溶液中c(H+)和c(OH-)的关系,下列说法正确的是( )
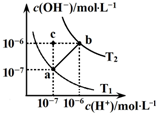

| A、ab线上任意点溶液均显中性 | B、b点时,溶液的pH=6,显酸性 | C、图中温度T1>T2 | D、在水中通入适量HCl气体可从a点变到c点 |
一定温度下,满足下列条件的溶液一定呈酸性的是( )
| A、pH=6的某物质的水溶液 | B、加酚酞后显无色的溶液 | C、能与金属Al反应放出H2的溶液 | D、c(H+)>c(OH-)的任意物质的水溶液 |
下列说法正确的是( )
| A、100℃时,KW=10-12,此温度下PH=6的溶液一定显酸性 | B、25℃时,0.1mol/L的NaHSO3溶液pH=4,说明HSO3-在水溶液中只存在电离 | C、NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用 | D、25℃时,10mL 0.1mol/L CH3COOH溶液与5mL 0.1mol/L NaOH溶液混合,所得溶液中有2c(Na+)═c(CH3COO-)+c(CH3COOH) |
下列物质能促进水的电离的是( )
| A、小苏打 | B、醋酸 | C、乙醇 | D、氯化钠 |
常温下,下列溶液肯定呈酸性的是( )
| A、溶液中含有H+ | B、滴入酚酞试液后,溶液呈红色 | C、与金属铝反应放出氢气 | D、与金属铁反应放出氢气 |