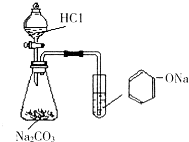
 关于图所示装置实验的说法中正确的是( )
关于图所示装置实验的说法中正确的是( )| A、可看到锥形瓶有气体产生,试管无现象 | B、可看到试管有白色沉淀产生,锥形瓶无现象 | C、该实验可以证明Na2CO3和C6H5ONa都易溶于水,C6H5OH不溶于水 | D、该实验可证明酸性强弱:盐酸>碳酸>苯酚 |
部分弱酸的电离平衡常数如表,下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、2CN-+H2O+CO2→2HCN+CO32- |
| B、2HCOOH+CO32-→2HCOO-+H2O+CO2↑ |
| C、中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
| D、等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者 |
下列说法正确的是( )
| A、强电解质一定可溶于水 | B、弱电解质是指部分溶于水的化合物 | C、弱电解质的导电性一定弱 | D、强酸、强碱不一定抑制弱酸弱碱的电离 |
下列物质中,属于弱电解质的是( )
| A、CH3COOH | B、H2SO4 | C、NaOH | D、Na2CO3? |
下列说法正确的是( )
| A、离子化合物一定是强电解质,共价化合物一定是弱电解质 | B、CuSO4溶液、Al、Fe3O4、NaOH溶液在一定条件下两两反应可得到3种不同单质 | C、Fe2O3、Al2O3、Na2O2都是碱性氧化物 | D、HClO、KMnO4、O3、H2O2不可能归为一类 |
下列事实一定能证明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④常温下0.1mol?L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的HNO2溶液稀释至100倍,pH约为3.1.
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④常温下0.1mol?L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的HNO2溶液稀释至100倍,pH约为3.1.
| A、①④⑥ | B、①②④⑤⑥ | C、①④⑤⑥ | D、全部 |
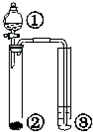
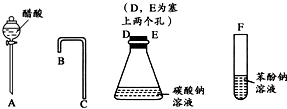 设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH.
设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH.