下列说法中,正确的是( )
①同种元素的原子的性质相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③胶体与溶液的本质区别是胶体具有丁达尔现象
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥食盐可以融冰化雪,用食盐作融雪剂不会对环境、植物生长产生任何危害
⑦1mol NH2-中含电子数为9NA.
①同种元素的原子的性质相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③胶体与溶液的本质区别是胶体具有丁达尔现象
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥食盐可以融冰化雪,用食盐作融雪剂不会对环境、植物生长产生任何危害
⑦1mol NH2-中含电子数为9NA.
| A、①③④ | B、①④⑥⑦ | C、②⑤ | D、①⑤⑦ |
下列说法正确的是( )
| A、常温下,反应4Fe(OH)2(s)+O2(g)+2H2O(l)=4Fe(OH)3(s)的△H<0、△S<0 | B、在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | C、锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用酸除去 | D、将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3 |
 Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工业上常利用醋酸和乙醇合成有机溶剂乙酸乙酯:CH3COOH(l)+C2H5OH(l)| 浓H2SO4 |
| △ |
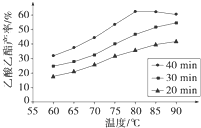
已知CH3COOH、C2H5OH和CH3COOC2H5的沸点依次为118℃、78℃和77℃.在其他条件相同时,某研究小组进行了多次实验,实验结果如图所示.(1)该研究小组的实验目的是
(2)60℃下反应40min与70℃下反应20min相比,前者的平均反应速率
(3)如图所示,反应时间为40min、温度超过80℃时,乙酸乙酯产率下降的原因可能是
Ⅱ.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)??H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
C(s)+H2O(g)??CO(g)+H2(g) 平衡常数为K1;
CO(g)+H2O(g)??H2(g)+CO2(g) 平衡常数为K2;
则K、K1、K2之间的关系是
(3)在V L密闭容器中通入10mol CO和10mol水蒸气,在T℃达到平衡,然后急速通过碱石灰,将所得混合气体燃烧,测得放出的热量为2 842kJ(已知CO燃烧热为283kJ?mol-1,H2燃烧热为286kJ?mol-1),则T℃平衡常数K=
反应CO(g)+2H2(g)?2CH3OH(g)在密闭容器中进行.为探究温度、CO2等对该反应的影响,进行了4组实验,结果如图.下列说法不正确的是( )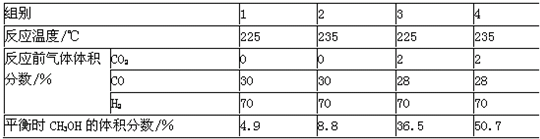

| A、该反应的△H>0 | B、当容器中压强不变时,反应达到平衡 | C、CH3OH含量增大的原因是CO2起了催化作用 | D、少量CO2能提高平衡时CH3OH的体积分数 |
为了检验某新型镍催化剂在不同温度下对苯催化加氢的影响.采用微型反应装置,在压强为0.78MPa,氢气和苯的物质的量之比为6.5:1的条件下不断升温,定时取样分析成分:
下列说法正确的是( )
| 温度/℃ | 85 | 90 | 95 | 100 | 200 | 280 | 300 | 320 | 340 |
| 苯(mmol) | 96.05 | 91.55 | 91.30 | 80.85 | 10 | 23.35 | 36.90 | 55.99 | 72.37 |
| 环己烷(mmol) | 3.95 | 8.45 | 8.7 | 19.15 | 90 | 76.65 | 63.10 | 44.01 | 27.63 |
| A、随着反应温度的升高,苯的反应速率先增大后减少 |
| B、通过改变温度或压强能使氢气和苯的转化率相同 |
| C、调控压强、氢气和苯的物质的量之比能提高苯的转化率 |
| D、当温度超过280℃,苯的转化率迅速下降,可能是因为温度过高催化剂活性下降 |
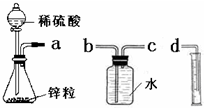 某化学实验小组的同学用下列仪器组装两套完全相同的装置定量探究浓度对反应速率的影响.
某化学实验小组的同学用下列仪器组装两套完全相同的装置定量探究浓度对反应速率的影响.(1)为达到本实验目的其装置连接顺序为:
a连
(2)连接好装置后的下一步操作是
(3)锥形瓶中发生反应的离子方程式为
(4)两套装置的分液漏斗所装的试剂分别为1mol/L硫酸和4mol/L硫酸,该小组同学要测定并记录的数据如下表:
| 加入的试剂 | H2的体积(相同条件下) | 反应时间 | 反应速率 |
| 1mol/L硫酸 | 10mL | t1 | v1 |
| 4mol/L硫酸 | 10mL | t2 | v2 |
(5)另有一组同学测定了每隔一分钟,锥形瓶中硫酸的浓度,记录结果如下:
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 硫酸浓度(mol/L | 4.0 | 3.8 | 3.5 | 3.1 | 2.6 | 2.2 | 1.9 | 1.8 | … |
请解释0到4mim时该化学反应速率随时间变化的原因:
(6)除上述实验方案可定量测定该反应的化学反应速率外,还可能有的实验测定方案有:
下面是某研究小组研究的关于不同催化剂对H2O2 分解反应的催化效率.
(1)写出H2O2 在催化剂作用下分解反应的化学方程式
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是 ,等质量的固体催化剂,颗粒大小对催化效率有什么影响
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是
(4)对于FeCl3的催化作用,有人认为是Fe3+起催化作用,有人认为是Cl-,请你设计一个实验进行验证. .
| 催化剂(0.1g) | 活性炭 | FeCl3 | KI | MnO2颗粒状 | MnO2粉末状 |
| 前15s产生氧气的量(ml) | 5 | 11 | 7 | 8 | 11 |
| 前30s产生氧气的量(ml) | 8 | 16 | 11 | 11 | 21 |
| 前45s产生氧气的量(ml) | 11 | 20 | 15 | 18 | 35 |
| 前60s产生氧气的量(ml) | 15 | 24 | 20 | 26 | 49 |
(2)从上表可以得出:活性炭、FeCl3、KI 和MnO2(粉末状)几种催化剂中,催化效率由大到小的顺序是
(3)实验发现新鲜的动物肝脏对H2O2 的分解也有显著的催化作用,但当往溶液中加入盐酸,或给溶液加热时,就会失去催化能力,合理的解释是
(4)对于FeCl3的催化作用,有人认为是Fe3+起催化作用,有人认为是Cl-,请你设计一个实验进行验证.
常温下,将FeCl3溶液和KI溶液混合,发生如下反应:
2Fe3++2I-?2Fe2++I2
某研究小组为了证明FeCl3溶液和KI溶液的反应存在一定限度,设计了如下实验:取5mL 0.1mol?L-1 KI溶液,滴加0.1mol?L-1 FeCl3溶液5~6滴,充分反应后溶液呈黄褐色,加入2mL CCl4溶液,振荡后静置,取上层溶液,滴加KSCN试剂,观察实验现象.
已知:v(正)=k?cm(I-)?cn(Fe3+)(k为常数)
根据以上信息回答下列问题:
(1)能够证明反应存在限度的现象是 .加入四氯化碳的作用是 .
(2)甲同学按上述步骤进行实验,结果并未观察到预期现象,推测可能原因是反应后溶液中Fe3+浓度过低.为此,甲又做了下列对比实验,实验结果记录如下:
分析实验记录,甲认为导致Fe3+浓度过低的原因是 ;乙同学结合平衡移动的知识,认为还有一个原因是 .
(3)该反应的平衡常数表达式为 .
(4)已知改变I-、Fe3+的浓度,正反应速率对应数值如下表所示:
分析表中数据,I-浓度对反应速率的影响 Fe3+浓度对反应速率的影响(填“大于”、“小于”或“等于”),理由是(写出计算过程) .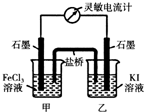
(5)现将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池
①能说明反应达到平衡的标志是 (填序号).
a.电流计读数为零 b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大 d.甲烧杯中溶液颜色不再改变
②反应达平衡后,向甲中加入适量FeCl2固体,此时 (填“甲“或“乙”)中石墨电极为负极,对应的电极反应方程式为 .
2Fe3++2I-?2Fe2++I2
某研究小组为了证明FeCl3溶液和KI溶液的反应存在一定限度,设计了如下实验:取5mL 0.1mol?L-1 KI溶液,滴加0.1mol?L-1 FeCl3溶液5~6滴,充分反应后溶液呈黄褐色,加入2mL CCl4溶液,振荡后静置,取上层溶液,滴加KSCN试剂,观察实验现象.
已知:v(正)=k?cm(I-)?cn(Fe3+)(k为常数)
根据以上信息回答下列问题:
(1)能够证明反应存在限度的现象是
(2)甲同学按上述步骤进行实验,结果并未观察到预期现象,推测可能原因是反应后溶液中Fe3+浓度过低.为此,甲又做了下列对比实验,实验结果记录如下:
| 氯化铁溶液用量 | 10滴 | 20滴 | 30滴 | 2mL | 3mL | 4mL |
| 萃取后上层溶液颜色 | 黄色 | 黄色 | 黄色 | 较深黄色 | 黄色略带红色 | 黄红色 |
| 加入KSCN溶液后颜色 | 不变红 | 不变红 | 略变红 | 偏血红色 | 血红色 | 血红色 |
(3)该反应的平衡常数表达式为
(4)已知改变I-、Fe3+的浓度,正反应速率对应数值如下表所示:
| c(I-)/mol?L-1 | c(Fe3+)/mol?L-1 | v/mol?L-1?s-1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |

(5)现将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池
①能说明反应达到平衡的标志是
a.电流计读数为零 b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大 d.甲烧杯中溶液颜色不再改变
②反应达平衡后,向甲中加入适量FeCl2固体,此时
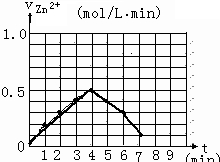
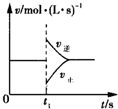 可逆反应2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )
可逆反应2SO2(g)+O2(g)?2SO3(g)△H<0,在一定条件下达到平衡状态,时间为t1时改变条件.化学反应速率与反应时间的关系如图所示.下列说法正确的是( )| A、维持温度、容积不变,t1时充入SO3(g) | B、维持压强不变,t1时升高反应体系温度 | C、维持温度、容积不变,t1时充入一定量Ar | D、维持温度、压强不变,t1时充入SO3(g) |
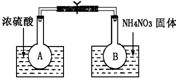 已知2NO2(g)═N2O4(g)△H=-52.7kJ?mol-1,常温下N2O4为无色气体.某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
已知2NO2(g)═N2O4(g)△H=-52.7kJ?mol-1,常温下N2O4为无色气体.某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验: