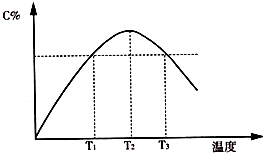
 在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中的C的含量与温度关系如图所示.下列说法正确的是( )
在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中的C的含量与温度关系如图所示.下列说法正确的是( )| A、此反应的正反应是吸热反应 | B、反应在T2温度时达到平衡 | C、T2温度时正反应速率大于逆反应速率 | D、T2温度时正反应速率大于T1温度时正反应速率 |
 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列叙述正确的是( )| A、反应的方程式为M?2N | B、t1时,N的浓度是M浓度的0.5倍 | C、t2时,正逆反应速率相等,达到平衡 | D、t3时,正反应速率大于逆反应速率 |
 在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入密闭容器中,发生反应.反应中各组分浓度随时间变化关系如图.下列说法中,正确的是( )
在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入密闭容器中,发生反应.反应中各组分浓度随时间变化关系如图.下列说法中,正确的是( )| A、a、b、c、d四个点中,只有b点的化学反应处于平衡状态 | B、前10min内用υ(NO2)表示的化学反应速率为0.04 mol/(L?min) | C、25min时,导致平衡移动的原因是升高温度 | D、a点,用υ(NO2)表示的化学反应速率等于用υ(N2O4)表示的化学反应速率 |
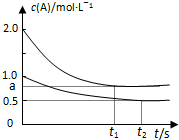 向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示:
向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示:| 容器 | 甲 | 乙 |
| 容积(L) | 0.5 | 0.5 |
| 反应放热(kJ) | Q1 | Q2 |
| 反应物起始量 | 1 molA 1 molB |
0.5 molA 0.5 molB |
| A、x=1 |
| B、Q1>2Q2 |
| C、根据题中信息无法计算a值 |
| D、保持其他条件不变,起始时向乙容器充入0.2mol A、0.2mol B、0.2mol C,则此时v(正)>v(逆) |
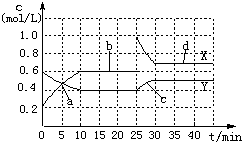 已知:2NO2?N2O4△H<0.现将混有少量NO2的N2O4气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如图所示.根据图分析,则下列说法正确的是( )
已知:2NO2?N2O4△H<0.现将混有少量NO2的N2O4气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如图所示.根据图分析,则下列说法正确的是( )| A、a、b、c、d四个点中的处于平衡状态的点是bd | B、前10min内v(NO2)=0.4 mol?L-1?min-1 | C、若要达到与15min相同的平衡状态,在25min时可采取的措施是加入催化剂或升高温度 | D、反应进行至25min时,曲线发生变化的原因是加入了0.4molNO2 |
可逆反应:mA(s)+nB(g)?eC(g)+fD(g),在反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图1图2所示.下列叙述正确的是( )
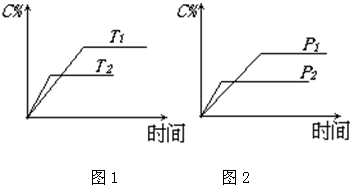

| A、达到平衡后,若升高温度,平衡向逆反应方向移 | B、达到平衡后,增加A的量有利于平衡向正反应方向移动 | C、达到平衡后,加入催化剂则C%增大 | D、化学方程式中n>e+f |
 已知NO2与N2O4相互转化:2NO2(g)?N2O4(g);△H=-24.4kJ/mol
已知NO2与N2O4相互转化:2NO2(g)?N2O4(g);△H=-24.4kJ/mol在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2L的密闭容器中,其中物质的浓度随时间变化的关系如图.下列推理分析合理的是( )
| A、前10min内,用v(NO2)表示的该反应速率为0.02mol/L?min | B、反应进行到10min时,体系吸收的热量为9.76kJ | C、a,b,c,d四点中c正与v逆均相等 | D、25min时,导致平衡移动的原因是升温 |
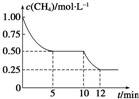 在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断不正确的是( )
在密闭容器中进行反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,测得c(CH4)随反应时间(t)的变化如图所示.下列判断不正确的是( )| A、10min时,改变的外界条件可能是升高温度 | B、0~10min内,v(H2)=0.15mol?L-1?min-1 | C、恒温下,缩小容器体积,一段时间内v逆>v正 | D、12min时,反应达平衡的本质原因是气体总质量不再变化 |
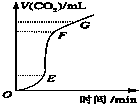 用纯净的CaCO3与稀盐酸反应制CO2,实验过程记录如图所示.根据分析判断正确的是( )
用纯净的CaCO3与稀盐酸反应制CO2,实验过程记录如图所示.根据分析判断正确的是( )| A、OE段表示反应速率最快 | B、EF段表示反应速率最快,收集的CO2最多 | C、FG段表示收集的CO2最多 | D、OG段表示随着时间的推移,反应速率逐渐增快 |
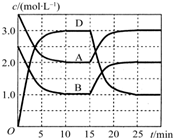 温度为T时,向2V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g);△H>0,容器中A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )
温度为T时,向2V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)?C(s)+xD(g);△H>0,容器中A、B、D的物质的量浓度随时间的变化如图所示.下列说法正确的是( )| A、反应在前10min的平均反应速率v(D)=0.15mol?L-1?min-1 | ||
B、该反应的平衡常数表达式K=
| ||
| C、若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动 | ||
| D、反应至15min时,改变的条件是降低温度 |