在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:则下列说法正确的是( )
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A、该反应的焓变为△H<0 |
| B、830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,扩大容器的体积.平衡向逆反应方向移动 |
| C、若1200℃时,某时刻体系中CO2、H2、CO、H2O的浓度分别为2 mol?L-1、2 mol?L-1、4 mol?L-1、4 mol?L-1,则此时v逆<v正 |
| D、若 830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,CO转化率为83.3% |
反应物和生成物均为气态的平衡体系,平衡常数表达式为:K=
,有关该平衡体系说法不正确的是( )
| c(x)?c2(y) |
| c3(z)?c2(w) |
| A、升高温度,该反应平衡常数K的变化无法判断 |
| B、增大压强,W的质量分数减小 |
| C、该反应的化学方程式为:2z(g)+2w(g)?x(g)+2y(g) |
| D、增大X气体浓度平衡向正反应方向移动 |
高炉炼铁过程中发生的反应:
Fe2O3(s)+CO(g)?
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下表,下列说法不正确的是( )
| 1 |
| 3 |
| 2 |
| 3 |
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
| A、△H<0 | ||
B、该反应的平衡常数表达式是K=
| ||
| C、其他条件不变,向平衡体系充入CO2气体,K值减小 | ||
| D、其他条件不变,升高温度,可以降低CO的平衡转化率 |
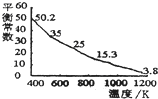 碘单质难溶于小却易溶于KI溶液.碘水中加入KI溶液发生反应:I2(aq)+I-(aq)?I3-(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )
碘单质难溶于小却易溶于KI溶液.碘水中加入KI溶液发生反应:I2(aq)+I-(aq)?I3-(aq),该反应的平衡常数与温度的关系如图,下列说法不正确的是( )| A、上述正反应为放热反应 | B、上述体系中加入苯,平衡不移动 | C、可运用该反应原理除去硫粉中少量的碘单质 | D、实验室配制碘水时,为增大碘单质的溶解度可加入适量KI溶液 |
在温度t1和t2(已知t2>t1)下,X2(g)和 H2反应生成HX的平衡常数如表所示,依据K的变化,随着卤素原子序数的递增,下列推断不正确的是( )
| 化学方程式 | K (t1) | K (t2) |
| F2+H2?2HF | 1.8×1036 | 1.9×1032 |
| Cl2+H2?2HCl | 9.7×1012 | 4.2×1011 |
| Br2+H2?2HBr | 5.6×107 | 9.3×106 |
| I2+H2?2HI | 43 | 34 |
| A、X2与H2反应的剧烈程度逐渐减弱 |
| B、HX的稳定性逐渐减弱 |
| C、HX的生成反应是放热反应 |
| D、在相同条件下,平衡时X2的转化率逐渐降低 |
下列叙述不正确的是( )
| A、化学平衡发生移动,平衡常数不一定发生变化 | B、升高温度会增大化学反应速率,其原困是增加了活化分子的百分数 | C、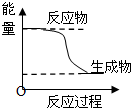 某化学反应的能量变化如图所示,则该反应的△H>0.△S>0 | D、H3PO4的电离常数:Kal>>Ka2>>Ka3 |
人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应:CO+HbO2?O2+HbCO,37℃时,该反应的平衡常数K=220.HbCO的浓度达到HbO2浓度的0.02倍,会使人智力受损.据此,下列结论错误的是( )
| A、CO与HbO2反应的平衡常数K=[O2]?[HbCO]/[CO]?[HbO2] | B、人体吸入的CO越多,与血红蛋白结合的O2越少 | C、若吸入的CO与O2浓度之比等于0.001时,人的智力会受损 | D、把CO中毒病人放入高压氧仓中解毒,目的是:使平衡常数减小,且向逆移动 |
某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表:
(1)根据上述数据分析,你认为 时间段(指0~1、1~2、2~3、3~4、4~5min,下同)的反应速率最大,收集的氢气最多. 时间段的反应速率最小.
(2)根据上述数据分析,锌与盐酸反应过程中的速率变化是开始时的速率逐渐加快,其影响因素是 .一定时间后反应速率逐渐减慢,其原因是 .
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是(填字母) .
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4.
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(累计值) | 50 | 120 | 232 | 290 | 310 |
(2)根据上述数据分析,锌与盐酸反应过程中的速率变化是开始时的速率逐渐加快,其影响因素是
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是(填字母)
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4.
某研究性活动小组用镁粉、盐酸、醋酸设计了以下实验,对两种酸分别与镁粉反应的速率和电离平衡进行研究.实验装置图如图(夹持固定装置已略去),正确操作得到如表实验数据.

分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,有同学发现该装置在设计上存在明显缺陷,根本无法完成实验,甚至存在危险,缺陷在于 ,经小组研究后,稍作改进就可以继续实验了,改进方法是 .
(2)改进装置后,如何检查其中一侧装置的气密性 .
(3)欲准确配制100ml0.10mol/L的盐酸,除需要烧杯、酸式滴定管之外,还需要用到的玻璃仪器有 .
(4)t(a1)>t(b1)的原因是 .
(5)请解释t(b3)-t(b2)值比t(b4)-t(b3)值大的原因是 .
(6)该实验可得出什么结论(最少答出两点)
①
②
③
(7)实验室用过量锌与盐酸制取氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入
A 冰醋酸 B 醋酸钠固体 C 石灰石 D 铜 E 烧碱 F 水 G 食盐溶液.

| A烧瓶中 | B烧瓶中 | 20℃、101kPa量筒(50ml)内气体体积 | 反应时间 | |
| A瓶 | B瓶 | |||
| 40ml0.1mol/L CH3COOH溶液 |
40ml0.1mol/L 盐酸溶液 |
5ml | t(a1)=155s | t(b1)=7s |
| 10ml | t(a2)=310s | t(b2)=16s | ||
| 15ml | t(a3)=465s | t(b3)=30s | ||
| 20ml | t(a4)=665s | t(b4)=34s | ||
(1)组装完成后,有同学发现该装置在设计上存在明显缺陷,根本无法完成实验,甚至存在危险,缺陷在于
(2)改进装置后,如何检查其中一侧装置的气密性
(3)欲准确配制100ml0.10mol/L的盐酸,除需要烧杯、酸式滴定管之外,还需要用到的玻璃仪器有
(4)t(a1)>t(b1)的原因是
(5)请解释t(b3)-t(b2)值比t(b4)-t(b3)值大的原因是
(6)该实验可得出什么结论(最少答出两点)
①
②
③
(7)实验室用过量锌与盐酸制取氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入
A 冰醋酸 B 醋酸钠固体 C 石灰石 D 铜 E 烧碱 F 水 G 食盐溶液.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法研究反应速率的有关问题.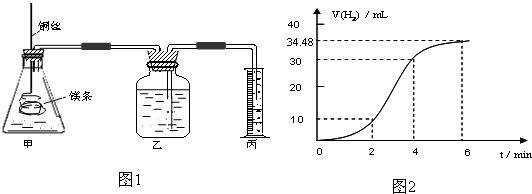
(1)实验1 探究Mg与盐酸反应速率的变化规律.取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是 .(填代号)
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为 .(假设图2氢气体积均已换算为标准状况下的体积,且溶液体积变化可忽略)
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响
已知MnO2+H2O2+2H+═Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
①上表中V1= mL,V3= mL.
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是 .
③若实验测得t2>t3>t4,则可得出的实验结论是 .
0 60545 60553 60559 60563 60569 60571 60575 60581 60583 60589 60595 60599 60601 60605 60611 60613 60619 60623 60625 60629 60631 60635 60637 60639 60640 60641 60643 60644 60645 60647 60649 60653 60655 60659 60661 60665 60671 60673 60679 60683 60685 60689 60695 60701 60703 60709 60713 60715 60721 60725 60731 60739 203614

(1)实验1 探究Mg与盐酸反应速率的变化规律.取一段镁条,用砂纸擦去表面的氧化膜,铜丝缠着镁条伸入装置甲中,使镁条浸入锥形瓶内的体积为2L稀盐酸(足量)中.镁条和盐酸反应生成H2的体积与反应时间的关系曲线如图2所示.
①从图2中看出0-6min内平均反应速率最快的时间段是
A.0-2min B.2-4min C.4-6min
②请计算4-6min 时间内,用HCl表示的平均反应速率为
③图1装置甲中与镁条相连的铜丝若一起浸入稀盐酸中对反应速率影响下列说法正确的是
A.加快反应速率但生成氢气的总量不变 B.减慢反应但增大生成氢气总量
C.不影响反应速率 D.加快反应速率但生成氢气的总量减小
(2)实验2 探究酸浓度对MnO2与H2O2反应速率的影响
已知MnO2+H2O2+2H+═Mn2++O2↑+2H2O,现取等量MnO2和下表有关物质,在相同温度下进行4组实验,分别记录收集20.0mL氧气所需时间.
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
②有同学提出实验I不可作为实验Ⅱ、Ⅲ、Ⅳ的对比实验,其理由是
③若实验测得t2>t3>t4,则可得出的实验结论是