在同温同压下,下列各组热化学方程式中,△H1>△H2的是( )
| A、S(g)+O2(g)=SO2(g),△H1;S(s)+O2(g)=SO2(g),△H2 | ||
| B、2H2(g)+O2(g)=2H2O(g),△H1;2H2(g)+O2(g)=2H2O(l),△H2 | ||
C、C(s)+
| ||
| D、H2(g)+Cl2(g)=2HCl(g),△H1;2H2(g)+2Cl2(g)=4HCl(g),△H2 |
已知:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ?mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol?L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为( )
| A、△H1=△H2 | B、△H2>△H1 | C、△H3>△H2 | D、△H1>△H3 |
已知红磷通常要比白磷稳定,下列两个反应:①P4(白磷,s)+5O2(g)═2P2O5(s)△H1②4P(红磷,s)+5O2(g)═2P2O5(s)△H2,则△H1和△H2的关系是( )
| A、△H1<△H2 | B、△H1>△H2 | C、△H1=△H2 | D、无法确定 |
在相同条件下,2mol C燃烧生成2mol CO放出的热量为Q1,2mol C 燃烧生成2mol CO2放出的热量为Q2,Q1和Q2的关系是( )
| A、Q1=Q2 | B、Q1>Q2 | C、Q1<Q2 | D、无法确定 |
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)→H2O(l)+57.3kJ,向1L 0.5mol/L的NaOH溶液中加入稀醋酸、浓硫酸、稀硝酸,则恰好完全反应时的热效应Q1、Q2、Q3的关系正确的是( )
| A、Q1<Q2<Q3 | B、Q1>Q3>Q2 | C、Q2>Q1>Q3 | D、Q1<Q3<Q2 |
盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是( )
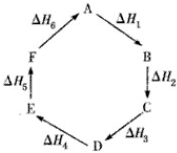

| A、C→F,|△H|=|△H1+△H2+△H6| | B、△H1+△H2+△H3+△H4+△H5+△H6=0 | C、A→F,△H=△H6 | D、|△H1+△H2+△H3|=|△H4+△H5+△H6| |
在101kPa和25℃时,有关反应的热化学方程式如下:
C(s)+
O2(g)=CO(g)△H1=-111kJ?mol-1
H2(g)+
O2(g)=H2O(g)△H2=-242kJ?mol-1
C(s)+O2(g)=CO2(g)△H3=-394kJ?mol-1
在同条件下,CO(g)+H2O(g)=H2(g)+CO2(g)△H,则△H是( )
C(s)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
C(s)+O2(g)=CO2(g)△H3=-394kJ?mol-1
在同条件下,CO(g)+H2O(g)=H2(g)+CO2(g)△H,则△H是( )
| A、-41kJ?mol-1 |
| B、+41kJ?mol-1 |
| C、-152kJ?mol-1 |
| D、-263kJ?mol-1 |