下列说法正确的是( )
| A、气化、液化和干馏是煤综合利用的主要方法,这三者中只有干馏是化学变化 | B、减少酸雨产生的途径是把工厂烟囱造高 | C、淀粉和纤维素都没有还原性,但在强酸中均可以水解得到具有还原性的物质 | D、醋酸纤维、硝化纤维、合成纤维、光导纤维都可由纤维素在一定条件下制得 |
下列关于化学与生产、生活的认识不正确的是( )
| A、普通铅笔芯的主要成分是铅 | B、煤的气化和液化过程均属化学变化 | C、硅酸钠溶液俗名水玻璃,可用于制备硅胶和木材防火剂 | D、合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺 |
下列有关煤的说法中不正确的是( )
| A、煤是工业上获得芳香烃的重要来源 | B、开发新能源,减少燃煤,是控制酸雨,保护环境的有效途径之一 | C、煤、石油、水煤气均是可再生能源 | D、煤的干馏和石油的裂解过程均属于化学变化过程 |
下列关于化石燃料的加工说法正确的是( )
| A、煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气 | B、煤制煤气是物理变化,是高效、清洁地利用煤的重要途径 | C、石油裂化主要得到乙烯 | D、石油分馏是化学变化,可得到汽油、煤油 |
下列关于有机物叙述不正确的是( )
| A、甲烷、甲苯、乙醇、乙酸都可以发生取代反应 | B、煤中含有苯、甲苯、二甲苯等芳香烃,可通过干馏制取 | C、蔗糖可以水解生成葡萄糖和果糖 | D、植物油通过加氢可以变为脂肪 |
下列与有机结构、性质相关的叙述中,正确的是( )
| A、分馏、干馏都是物理变化,裂化、裂解都是化学变化 | B、乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 | C、丹参素结构如图所示,能发生取代、加成、氧化反应 | D、淀粉、纤维素都用(C6H10O5)n表示,二者互为同分异构体 |
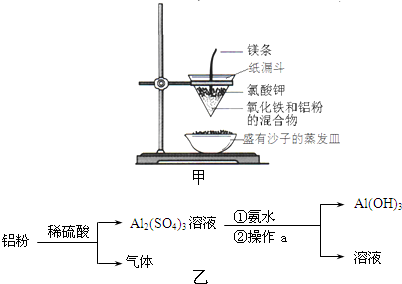
某研究性学习小组对铝热反应实验展开研究.现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”、“纸漏斗的下部被烧穿,有熔融物落入沙中”.查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3熔点、沸点数据如下:
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?答:
(填“合理”或“不合理”)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是
反应的离子方程式为 .
(3)实验室溶解该熔融物,下列试剂中最好的是 (填序号).
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
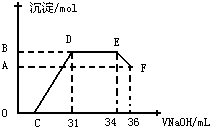
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为 上述现象说明溶液中 结合OH-的能力比 强(填离子符号).
(3)B点对应的沉淀的物质的量为 mol,C点对应的氢氧化钠溶液的体积为 mL.
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
(填“合理”或“不合理”)
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.该实验所用试剂是
反应的离子方程式为
(3)实验室溶解该熔融物,下列试剂中最好的是
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:

(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为
(3)B点对应的沉淀的物质的量为
铝热反应常用于冶炼高熔点的金属,可简单认为是铝与某些金属氧化物在高温条件下发生的反应.某学习小组对铝热反应(以Al和Fe2O3反应为例)实验进行研究.查阅数据得到Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下表所示:
试回答下列问题:
(1)在铝热反应中金属铝表现出 性(填“氧化”或“还原”).请判断下列金属中那一个不能由铝热反应制取 .(填序号)
①Fe ②Cr(铬) ③V(钒) ④Ca ⑤Mn
(2)某同学推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为 ,可观察到的实验现象是 .
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色未变血红色,即可证明熔融物中不含有Fe2O3.则
①物质甲是 (填化学式).
②该同学的实验方案是否合理? (填“合理”或“不合理”).理由: .
0 60457 60465 60471 60475 60481 60483 60487 60493 60495 60501 60507 60511 60513 60517 60523 60525 60531 60535 60537 60541 60543 60547 60549 60551 60552 60553 60555 60556 60557 60559 60561 60565 60567 60571 60573 60577 60583 60585 60591 60595 60597 60601 60607 60613 60615 60621 60625 60627 60633 60637 60643 60651 203614
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1565 |
| 沸点/℃ | 2467 | 2980 | 2750 | … |
(1)在铝热反应中金属铝表现出
①Fe ②Cr(铬) ③V(钒) ④Ca ⑤Mn
(2)某同学推测,铝热反应所得到的熔融物中应含有铁、铝两种金属.如设计一个简单的实验方案证明该熔融物中含有金属铝,则实验所需用的试剂为
(3)另一同学推测铝热反应得到的熔融物中还含有Fe2O3,他设计了如下方案来验证:
取一块该熔融物投入到少量稀硫酸中,向反应后的混合液中滴加物质甲的溶液,观察溶液颜色未变血红色,即可证明熔融物中不含有Fe2O3.则
①物质甲是
②该同学的实验方案是否合理?