下列有关化学反应速率的说法中,正确的是( )
| A、100mL2mol/L盐酸与锌反应时,加入100mL氯化钠溶液,生成氢气的速率不变 | B、对于可逆反应2CO+2NO?N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 | C、二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢 | D、用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生 |
把铝条放入到盛有过量稀盐酸的试管中,不影响氢气的产生速率的因素是( )
| A、盐酸的浓度 | B、铝条的表面积 | C、溶液的温度 | D、加入少量的硫酸钠 |
下列说法正确是( )
| A、影响反应速率大小的决定性因素是温度 | B、可逆反应达到化学平衡状态就是这个反应在该条件下所能达到的最大限度 | C、苯分子是一个由6个碳原子以单双键交替结合而成的六元环 | D、开发海洋资源可获得Fe、Co、K、Au、Mg、Br等金属 |
2SO2+O2
2SO3是接触法制硫酸工艺中的重要反应,下列关于该反应的说法中错误的是( )
| 一定条件 |
| A、增加SO2的浓度能加快该反应的速率 |
| B、通常使用铁作催化剂 |
| C、降低体系温度会减慢该反应的速率 |
| D、使用催化剂能改变该反应的速率 |
决定一个化学反应速率快慢的最主要因素是( )
| A、催化剂 | B、温度 | C、反应物本身性质 | D、浓度 |
四个试管中都装有5mL 0.1mol/LNa2S2O3溶液,分别在不同温度下加入0.1mol/L硫酸和一定量水,最先出现浑浊的是( )
| A、40℃,4 mL硫酸,1 mL水 | B、20℃,4 mL硫酸,1 mL水 | C、40℃,1 mL硫酸,4 mL水 | D、20℃,1 mL硫酸,4 mL水 |
一定条件下,可逆反应C(s)+CO2(g)?2CO(g)△H>0,达到平衡状态,现进行如下操作:①减少体系中CO的量;②缩小反应体系的体积;③增加反应物C(s)的用量;④升高反应体系的温度;上述措施中一定能使反应的正反应速率显著加快的是( )
| A、①②③④ | B、②④ | C、③④ | D、①②④ |
铝与稀硫酸反应的速率较慢,下列措施不能加快反应速率的是( )
| A、在溶液中滴加少量硫酸铜溶液 | B、适当增大硫酸的浓度 | C、对反应溶液进行加热 | D、增大外界压强 |
化学中常借助曲线图来表示某种变化过程,有人分别画出了下列的四个曲线图:
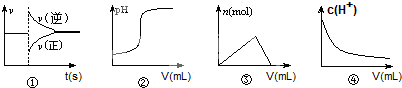
有关上述曲线图的说法正确的是( )

有关上述曲线图的说法正确的是( )
| A、曲线图①可以表示恒压容器中某化学平衡体系充入气体生成物后反应速率随时间的变化 | B、曲线图②可以表示向一定量的氢氧化钠溶液中滴加一定浓度的盐酸时的pH的变化 | C、曲线图③可以表示向一定量的明矾溶液中滴加一定浓度的氢氧化钡溶液时的产生沉淀的物质的量变化 | D、曲线图④可以表示冰醋酸加水稀释过程中溶液中c(H+)的变化 |
有效碰撞概念模型是研究化学反应速率的基础.下列说法中正确的是( )
| A、升高温度,有效碰撞次数增加 | B、发生有效碰撞时,不一定发生化学反应 | C、活化分子之间发生的碰撞一定为有效碰撞 | D、加入催化剂,分子能量不变,有效碰撞次数不变 |