下列说法正确的是( )
| A、当△H<0时,表示该反应为吸热反应 | B、相同条件下,溶液中Fe3+,Zn2+,Cu2+的氧化性依次减弱 | C、铅蓄电池在放电过程中,负极质量减小,正极质量增加 | D、钢铁吸氧腐蚀的正极电极反应:O2+2H2O+4e-═4OH- |
下列叙述不正确的是( )
| A、需要加热才能发生的反应不一定是吸热反应 | B、热化学方程式中的化学计量数表示物质的量,可以是分数 | C、应用盖斯定律可计算某些难以直接测量的反应焓变 | D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下△H不同 |
已知氢气和碳燃烧的热化学方程式为:
①2H2(g)+O2(g)═2H2O(l)△H1=-akJ?mol-1
②H2(g)+1/2O2(g)═H2O(g)△H2=-bkJ?mol-1
③C(s)+1/2O2(g)═CO(g)△H3=-ckJ?mol-1
④C(s)+O2(g)═CO2(g)△H4=-dkJ?mol-1
下列说法错误的是( )
①2H2(g)+O2(g)═2H2O(l)△H1=-akJ?mol-1
②H2(g)+1/2O2(g)═H2O(g)△H2=-bkJ?mol-1
③C(s)+1/2O2(g)═CO(g)△H3=-ckJ?mol-1
④C(s)+O2(g)═CO2(g)△H4=-dkJ?mol-1
下列说法错误的是( )
| A、氢气的燃烧热为△H=-akJ?mol-1 | B、c<d | C、一氧化碳的燃烧热为△H=-(d-c)kJ?mol-1 | D、0.5a>b |
下列利用相关数据作出的推理或判断一定正确的是( )
| A、利用焓变数据判断反应是否自发进行 | B、利用溶液的pH判断该溶液的酸碱性 | C、利用平衡常数判断反应进行的程度大小 | D、利用反应热数据判断反应速率的大小 |
下列说法正确的是( )
| A、焓变是指1mol物质参加反应时的能量变化 | B、△H的大小与热化学方程式的计量系数无关 | C、反应物和生成物所具有的能量差决定了反应是放热反应还是吸热反应 | D、需要加热才能发生的反应一定是吸热反应 |
根据图提供的信息,下列所得结论不正确的是( )
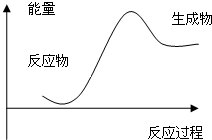

| A、反应物比生成物稳定 | B、该图可以表示石灰石高温分解 | C、该反应的△H>0 | D、因为生成物的总能量高于反应物的总能量该反应一定需要加热 |
下列说法正确的是( )
| A、凡经加热而发生的化学反应都是吸热反应 | B、干冰升华时,二氧化碳分子中的共价键不发生断裂 | C、C(石墨,s)=C(金刚石,s),反应中既没有电子得失也没有能量变化 | D、伴有能量变化的物质变化,都是化学变化 |
下列说法中正确的是( )
| A、吸热反应在不加热的条件下一定不能发生 | B、放热反应在常温下一定很容易发生 | C、化学变化中的能量变化主要由化学键变化引起的 | D、化学反应中的能量变化,只表现为热能的变化 |
下列关于判断过程的方向的说法正确的是( )
| A、所有自发进行的化学反应都是放热反应 | B、判断化学反应能否自发进行,必须综合考虑反应的焓变和熵变 | C、自发反应一定是熵增大,非自发反应一定是熵减小的反应 | D、同一物质的固、液、气三种状态中固体的熵值最大 |
指出下列说法正确的是( )
| A、生物体内进行的缓慢氧化反应是放热反应 | B、化学键形成时释放的能量越多,化学键越活泼 | C、需要加热条件的化学反应都是吸热反应 | D、1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 |