根据热化学方程式(在101kPa时)S(s)+O2(g)=SO2(g)△H=-297.23kJ/mol,分析下列说法中不正确的是( )
| A、S的燃烧热为297.23 kJ/mol | B、S(g)+O2(g)=SO2(g) 1mol S(g)放出的热量大于297.23kJ | C、S(g)+O2(g)=SO2(g) 1mol S(g)放出的热量小于297.23kJ | D、形成1mol SO2的化学键释放的总能量大于断裂1mol S(s) 和1mol O2(g) 的化学键所吸收的总能量 |
已知反应:
①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol
下列结论正确的是( )
| A、碳的燃烧热的数值大于110.5kJ/mol | B、①的反应热为221kJ/mol | C、1molH+(aq)与1mol OH-(aq)的总能量高于1mol H2O(l)的能量 | D、浓硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol |
 某化学反应过程中的能量变化关系如图所示,下列结论正确的是( )
某化学反应过程中的能量变化关系如图所示,下列结论正确的是( )| A、该反应是放热反应 | B、生成物的总能量小于反应物的总能量 | C、该反应中其他形式的能量转化成了化学能 | D、该反应可能是酸和碱的中和反应 |
下列反应中,生成物的总能量大于反应物的总能量的是( )
| A、氢气在空气中燃烧 | B、氢氧化钡晶体与氯化铵晶体反应 | C、盐酸与氨氧化钠溶液反应 | D、锌与稀硫酸反应制取氢气 |
已知反应:①2C(s)+O2(g)=2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
| A、碳的燃烧热是110.5kJ/mol | B、反应①的反应热为221kJ/mol | C、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3 kJ热量 | D、稀盐酸与稀NaOH溶液反应的中和热为57.3 kJ/mol |
根据如图提供的信息,下列所得结论不正确的是( )
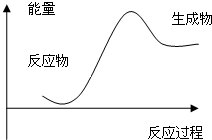

| A、反应物比生成物稳定 | B、该图可以表示石灰石高温分解 | C、该图可以表示断开反应物中的化学键吸收的能量大于形成生产物中的化学键放出的能量 | D、因为生成物的总能量高于反应物的总能量,所以该反应一定需要加热 |
石墨在一定条件下可转化为金刚石,已知12g石墨完全转化为金刚石时,要吸收QkJ的热量,下列说法正确的是( )
| A、石墨不如金刚石稳定 | B、金刚石与石墨的结构是相同的 | C、等物质的量的石墨与金刚石完全燃烧,金刚石放出的热量多 | D、等物质的量的石墨与金刚石完全燃烧,石墨放出的热量多 |
碘与氢气一定条件下反应的热化学方程式如下,下列判断正确的是( )
(Ⅰ) I2(g)+H2(g)?2HI(g)△H=-9.48KJ/mol
(Ⅱ) I2(s)+H2(g)?2HI(g)△H=+26.48KJ/mol.
(Ⅰ) I2(g)+H2(g)?2HI(g)△H=-9.48KJ/mol
(Ⅱ) I2(s)+H2(g)?2HI(g)△H=+26.48KJ/mol.
| A、2 g H2(g)通入254 g I2(g) 中在该条件下反应的反应放热为9.48 kJ | B、1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ | C、反应(Ⅰ)的产物比反应(Ⅱ)的产物稳定 | D、物质的量相同时,反应(Ⅰ)的反应物总能量比反应(Ⅱ)的反应物总能量高 |
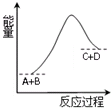 已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )| A、该反应为吸热反应 | B、A物质能量一定低于C物质能量 | C、该反应只有在加热条件下才能进行 | D、反应物的总能量高于生成物的总能量 |
下列叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 | B、需要加热才能发生的反应一定是吸热反应 | C、反应是放热反应还是吸热反应,由生成物与反应物的焓值差决定 | D、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |