下列有关说法正确的是( )
| A、0.1mol/L Na2CO3溶液35℃时的碱性比25℃时强,说明盐类水解反应是放热反应 | B、从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增的规律 | C、2SO2(g)+O2(g)?2SO3(g)△H<0,其它条件不变时加入催化剂,反应速率v(SO2)和SO2转化率均增大 | D、室温下,同浓度的Na2CO3溶液的pH比Na2SiO3溶液的pH大,说明非金属性C>Si |
设NA为阿伏伽德罗常数的值,对反应
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=a kJ/mol
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=b kJ/mol,其它数据如表:
下列说法正确的是( )
(1)CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=a kJ/mol
(2)CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2=b kJ/mol,其它数据如表:
| 化学键 | C═O | O═O | C-H | O-H |
| 键能kJ?mol-1 | 798 | x | 413 | 463 |
| A、H2O(g)═H2O(l)△S<0,△H═a-b kJ/mol | ||
| B、当有4NA个C-H键断裂时,该反应放出热量一定为a kJ | ||
C、如表中 x=
| ||
| D、利用反应(1)设计的原电池电解精炼铜时,当负极输出0.2NA个电子时,电解槽的阳极一定减轻6.4g |
根据如图所示的N2(g)和02(g)反应生成NO(g)过程中的能量变化情况,判断下列说法正确的是( )
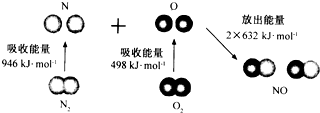

| A、N2(g)和02(g)反应生成NO(g)是放热反应 | B、2mol O原子结合生成O2(g)时需要吸收498kJ能量 | C、1mol NO(g)分子中的化学键断裂时需要吸收632kJ能量 | D、N2(g)+02(g)═2NO(g)的反应热△H=+1444kJ?mol-1 |
下列反应属于吸热反应的是( )
| A、钠与水反应 | B、碳与CO2的反应 | C、H2与Cl2的反应 | D、NaOH与盐酸的反应 |
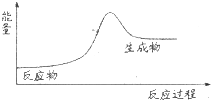 下列反应中的能量变化关系符合如图所示的是( )
下列反应中的能量变化关系符合如图所示的是( )| A、盐酸与烧碱反应 | B、天然气燃烧 | C、三氧化硫与水反应 | D、煅烧石灰石 |
下列有关叙述正确的是( )
| A、需要加热才能发生的反应一定是吸热反应 | B、强电解质溶液的导电能力一定比弱电解质溶液的强 | C、SO3溶于水,其水溶液能导电,故SO3是电解质 | D、升高温度,可提高活化分子百分数,使有效碰撞增多,化学反应速率加快 |
下列反应中生成物总能量高于反应物总能量的是( )
| A、铝粉与氧化铁粉末反应 | B、乙醇燃烧 | C、碳酸钙受热分解 | D、氧化钙溶于水 |
下列反应属于吸热反应的是( )
A、 | B、 | C、 | D、 |
下列反应属于吸热反应的是( )
| A、Ba(OH)2?8H20晶体和NH4Cl混合搅拌 | B、盐酸和氢氧化钠溶液混合 | C、锌放入稀硫酸中 | D、生石灰和水在常温下反应 |
下列反应属于吸热反应的是( )
| A、反应物的总能量大于生成物的总能量 | B、CH3COOH+KOH?CH3COOK+H2O | C、破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量 | D、C6H12O6(葡萄糖aq)+6O2→6CO2+6H2O |