下列关于化学键的叙述正确的是( )
| A、离子化合物中只含离子键 | B、共价化合物一定不含离子键 | C、离子化合物一定不含共价键 | D、共价化合物可能含有离子键 |
下列变化中,不需要破坏化学键的是( )
| A、氯化氢气体溶于水 | B、氯化钠溶于水 | C、加热氯酸钾使其分解 | D、碘升华 |
下列物质属于离子化合物且含有共价键的是( )
| A、HCl | B、NaCl | C、NaOH | D、H2O |
下列说法中正确的是( )
| A、离子化合物中可以含有共价键,但共价化合物中一定不含离子键 | B、含有共价键的物质一定是共价化合物 | C、分子中一定含有化学键 | D、含有金属元素的离子一定是阳离子 |
下列变化中,不需要破坏化学键的是( )
| A、氧化钠溶于水 | B、氯化铵溶于水 | C、氯化氢溶于水 | D、冰熔化 |
化学键使得一百多种元素构成了世界万物.关于化学键的下列叙述中,正确的是( )
| A、化学键是相邻原子或离子间的相互作用,它存在于分子、原子团中 | B、离子键是阴、阳离子通过静电作用而形成的化学键 | C、共价键只存在于共价化合物中 | D、非金属元素的原子之间不可能形成离子键 |
下列叙述正确的是( )
| A、两种非金属元素的原子之间形成的化学键都不是非极性键 | B、两种元素构成的共价化合物分子中的化学键都是极性键 | C、含有极性键的化合物分子中一定不含非极性键 | D、只要是离子化合物,其熔点就比共价化合物的熔点高 |
下列物质发生变化时,共价键未被破坏的是( )
| A、氯化氢溶于水 | B、氯化铵受热分解 | C、金刚石转化为石墨 | D、干冰的升华 |
已知2-氨基丙酸铵结构如图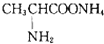 ,下列叙述正确的是( )
,下列叙述正确的是( )
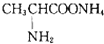 ,下列叙述正确的是( )
,下列叙述正确的是( )| A、该物质中只含有共价键 | B、-NH2可以与H2O形成氢键 | C、该物质难溶于水 | D、该物质的晶体属于分子晶体 |
下列说法错误的是( )
| A、H2O2和Na2O2都属于氧化物,两种物质中所含的化学键类型完全相同 | B、原子核外在离核较远区域的电子易失去,其原因是这些电子能量较高 | C、第三周期非金属元素形成氢化物的稳定性从左到右逐渐增强 | D、在周期表的金属元素和非金属元素的交界处寻找半导体,在过渡元素区中寻找催化剂 |