砷是第4周期第ⅤA族非金属元素,下列关于砷的推测不正确的是( )
| A、属于短周期元素 | B、可以存在-3、+3、+5等多种化合价 | C、砷在通常情况下是固体 | D、最高价氧化物As2O5属于酸性氧化物 |
如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
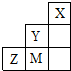
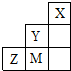
| A、离子半径:M->Z2->Y- | B、Z元素形成的氧化物都是共价化合物 | C、气态氢化物稳定性:Y>Z>M | D、三种元素中,M的最高价氧化物对应的水化物酸性最强 |
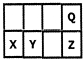 短周期元素X、Y、Z、Q在元素周期表中的相对位置如图地壳中含量最大的三种元素已包含其中.关于这些元素的叙述不合理的是( )
短周期元素X、Y、Z、Q在元素周期表中的相对位置如图地壳中含量最大的三种元素已包含其中.关于这些元素的叙述不合理的是( )| A、最高价氧化物对应水化物的酸性Z>Y | B、原子半径X>Y | C、一定条件下,Q可分别与X、Y、Z形成化合物,这些化合物都可溶于NaOH溶液 | D、元素Y的氧化物是形成酸雨的罪魁祸首 |
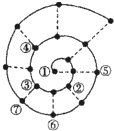 如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“?”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )| A、最简单气态氢化物的稳定性③比⑦小 | B、最高价氧化物对应小化物的酸性⑥比⑦弱 | C、金属性②比⑤弱 | D、原子半径③比④大 |
 如图是元素周期表的一部分,已知A、B、C、D、E均为短周期元素,D元素最外层电子数为最内层电子数的3倍,下列说法中正确的是( )
如图是元素周期表的一部分,已知A、B、C、D、E均为短周期元素,D元素最外层电子数为最内层电子数的3倍,下列说法中正确的是( )| A、元素A位于第二周期第ⅣA族 | B、原子半径:B>C | C、最高价氧化物对应水化物的酸性:C>E | D、气态氢化物的稳定性:D>B |
主族元素的化学性质主要取决于( )
| A、元素的化合价 | B、原子的质量数 | C、原子的最外层电子数 | D、原子半径 |
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A、原子半径:W>Z>Y>X |
| B、最高价氧化物对应水化物的酸性W比Z弱 |
| C、Y的气态氢化物的稳定性较Z的弱 |
| D、四种元素的单质中,Z的熔、沸点最高 |
下列关于元素周期表和元素周期律的说法错误的是( )
| A、Fe元素位于元素周期表的p区 | B、第三周期元素从Na到Cl,电负性、非金属性逐渐增强 | C、第IA族元素从Li到Cs,原子半径依次减小、第一电离能依次增大 | D、元素周期表中从IIIB族到IIB族10个纵行的元素都是金属元素 |
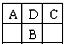 A、B、C为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法错误的是( )
A、B、C为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法错误的是( )| A、A的氧化物有多种形式 | B、B最高价氧化物对应的水化物是一种弱酸 | C、C的氢化物比HCl稳定 | D、D元素形成的单质不止一种 |
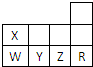 表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
表为元素周期表前三周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A、常压下五种元素的单质中Z单质的沸点最高 | B、Y、Z、W的阴离子的还原性强弱顺序为:Z->Y2->W3- | C、最高价含氧酸的酸性强弱顺序为:H2YO4>HZO4>H3WO4 | D、五种元素对应的单质固态时均为分子晶体 |