斤C、N、Si眉嶽圷殆議偃峰危列議頁↙ ⇄
| A、侭侃議巓豚會方⦿C=N〽Si | B、圻徨磯抄⦿Si﹅C﹅N | C、恷互晒栽勺⦿Si﹅C﹅N | D、掲署奉來⦿N﹅C﹅Si |
和双嗤購狽晒麗議偃峰嶄屎鳩議頁↙ ⇄
| A、壓賊晒狽嶄HF恷糧協 | B、匯倖D2O蛍徨侭根議嶄徨方葎8 | C、糧協來⦿H2S﹅HF | D、HCl議窮徨塀葎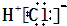 |
和双辛恬葎登僅S才Cl議掲署奉來膿樋卆象議頁↙ ⇄
| A、Cl2+H2S=S◎+2Cl- | B、磨來⦿H2SO4〽HClO | C、磨來⦿H2S〽HCl | D、葬圻徨議恷翌蚊窮徨方曳柁圻徨議富 |
和双購噐麗嵎來嵎延晒議曳熟嶄⇧音屎鳩議頁↙ ⇄
| A、磨來膿樋⦿HBrO4﹅HClO4 | B、圻徨磯抄寄弌⦿Na﹅S | C、珠來膿樋⦿NaOH﹅LiOH | D、珊圻來膿樋⦿F-〽Cl- |
和双傍隈嬬校傍苧紀議掲署奉來曳宋膿議頁↙ ⇄
| A、HNO3曳H3PO4厚糧協 | B、HNO3議剳晒來曳H3PO4膿 | C、HNO3議磨來曳H3PO4膿 | D、HNO3曳H3PO4否叟屍窟 |
和中偃峰屎鳩議頁↙ ⇄
| A、揖怛掲署奉圷殆⇧徭貧遇和侭侘撹議磨⇧凪磨來愁樋⇧咀葎掲署奉來愁樋 | B、揖怛掲署奉議恷詰勺咐宣徨⇧喇貧遇和凪珊圻來愁膿⇧遇剳晒來愁樋 | C、圷殆巓豚燕及15双議圷殆嗤⦿S、Se、Te吉 | D、壓圷殆巓豚燕議侭嗤怛嶄⇧‰B怛侭根議圷殆嶽窃恷謹 |
和双潤胎屎鳩議頁↙ ⇄
〙腺徨磯抄⦿S2-﹅Cl﹅S 〖狽晒麗糧協來⦿HF﹅HCl﹅PH3◉
〗宣徨珊圻來⦿S2-﹅Cl-﹅Br-﹅I- ∠汽嵎剳晒來⦿Cl2﹅S◉
⊥磨來⦿H2SO4﹅HClO4 ⌒珠來膿樋⦿KOH﹅NaOH﹅Mg↙OH⇄2⤴
〙腺徨磯抄⦿S2-﹅Cl﹅S 〖狽晒麗糧協來⦿HF﹅HCl﹅PH3◉
〗宣徨珊圻來⦿S2-﹅Cl-﹅Br-﹅I- ∠汽嵎剳晒來⦿Cl2﹅S◉
⊥磨來⦿H2SO4﹅HClO4 ⌒珠來膿樋⦿KOH﹅NaOH﹅Mg↙OH⇄2⤴
| A、〙 | B、〗⌒ | C、〖∠⌒ | D、〙〗∠ |
和双偃峰嶄屎鳩議頁↙ ⇄
| A、H2S議糧協來曳HF議糧協來膿 | B、蝶圷殆X議賑蓑狽晒麗議晒僥塀葎H2X⇧夸凪恷互勺剳晒麗議晒僥塀葎XO3 | C、宣徨晒栽麗嶄辛嬬根嗤慌勺囚⇧慌勺晒栽麗嶄辛嬬根嗤宣徨囚 | D、匯倖D2O蛍徨侭根議嶄徨方葎8 |
和双嗤購麗嵎來嵎議曳熟嶄⇧屎鳩議頁↙ ⇄
〙犯糧協來⦿CH4﹅NH3﹅H2O
〖珊圻來⦿I-﹅Br-﹅Cl-
〗珠來⦿NaOH﹅Mg↙OH⇄2﹅Al↙OH⇄3
∠唱悶議匪泣⦿O2﹅Na﹅Si⤴
〙犯糧協來⦿CH4﹅NH3﹅H2O
〖珊圻來⦿I-﹅Br-﹅Cl-
〗珠來⦿NaOH﹅Mg↙OH⇄2﹅Al↙OH⇄3
∠唱悶議匪泣⦿O2﹅Na﹅Si⤴
| A、〙〗 | B、〖∠ | C、〖〗 | D、〙∠ |
和双麗嵎來嵎曳熟屎鳩議頁↙ ⇄
| A、犯糧協來⦿HCl﹅H2S﹅H2O | B、宣徨磯抄⦿Na+﹅Cl匯﹅F- | C、珠來⦿NaOH﹅Mg↙OH⇄2﹅Al↙OH⇄3 | D、匪泣⦿署胡墳﹅孤甥﹅奮冦 |