元素周期律和元素周期表是学习化学的重要工具,下列说法中,不正确的是( )
| A、HF、HCl、HBr、HI的还原性依次增强,热稳定性依次减弱 | B、P、S、Cl得电子能力和最高价氧化物对应水化物的酸性均依次增强 | C、IA族的金属单质与水反应比同周期IIA族的金属单质剧烈 | D、除稀有气体外,第三周期元素的原子半径和离子半径随原子序数的增加而减小 |
下列叙述正确的是( )
| A、IA族金属元素是同周期中金属性最强的元素 | ||||
| B、不同元素的原子构成的分子中一定只含极性共价键 | ||||
C、
| ||||
| D、ⅦA族元素的简单阴离子还原性越强,其最高价氧化物对应水化物的酸性就越强 |
下列关于同主族元素的说法中错误的是( )
| A、同主族元素随原子序数递增,元素原子失电子能力逐渐增强 | B、同主族元素随原子序数递增,单质氧化性逐渐增强 | C、同主族元素原子最外层电子数都相同 | D、同主族元素的原子半径,随原子序数增大而逐渐增大 |
下列关于碳族元素的叙述,不正确的是( )
| A、碳族元素位于元素周期表的ⅣA族,原子最外层有4个电子 | B、随着核电荷数的递增,非金属性逐渐减弱、金属性逐渐增强 | C、随着核电荷数的递增,单质的熔沸点逐渐升高 | D、随着核电荷数的递增,最高价氧化物对应水化物的酸性逐渐增强 |
下列单质最容易与氢气发生化学反应的是( )
| A、Br2 | B、I2 | C、F2 | D、Cl2 |
已知16S和34Se位于同一主族,下列关系正确的是( )
| A、热稳定性:HF>HC1>H2S | B、原子半径:Br>Se>Cl | C、还原性:S2->Se2->Cl- | D、酸性:HBrO4>HClO4>H2SO4 |
铊是元素周期表中ⅢA族元素,下列关于铊的叙述不正确的是( )
| A、铊比铝的金属性更强 | B、铊能与盐酸反应放出氢气 | C、氢氧化铊一定具有两性 | D、铊在化合物中可以呈+3价 |
门捷列夫制作元素周期表时,许多元素尚未发现,他在铝的下面留了空位给“类铝”,并对“类铝”的性质进行了预测,“类铝”与后来发现的镓的性质一致,从而验证了元素周期表的正确性.下列有关镓的性质的描述中错误的是( )
| A、镓的金属性比铝弱 | B、镓的常见化合价为+3 | C、镓的原子半径比铝大 | D、镓的原子结构示意图为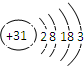 |
2007年6月20日,新浪网报道了中国矿业大学发生的铊中毒事件.铊(Tl )在元素周期表中与铝处于同一主族,与铯(Cs)处于同一周期.下列有关说法中正确的是( )
| A、201Tl与204Tl互为同素异形体 | ||||
B、
| ||||
| C、Tl核外有6个电子层 | ||||
| D、Tl原子半径大于Cs原子半径 |
a、b、c、d、e是第三周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的稳定性c>d,e的单质既能与氢氧化钠溶液反应,也能与稀硫酸反应,并且都产生氢气,则它们的原子序数由小到大的顺序是( )
| A、a、b、e、d、c | B、b、a、c、e、d | C、b、a、e、d、c | D、b、a、d、c、e |