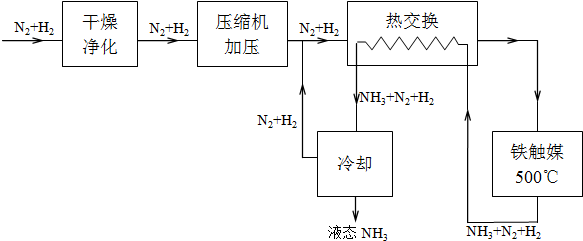
工业合成氨与制备硝酸一般可连续生产,流程如图:
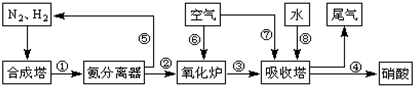
(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g)?CO2(g)+H2(g).t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气.反应建立平衡后,体系中c(H2)=0.12mol?L-1.则该温度下此反应的平衡常数K= (填计算结果).
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1 300℃(填“>”、“<”或“=”).
(3)氨气在纯氧中燃烧生成一种单质和水,科学家利用此原理,设计成“氨气-氧气”燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 .
(4)用氨气氧化可以生产硝酸,但尾气中的NOx会污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为 .
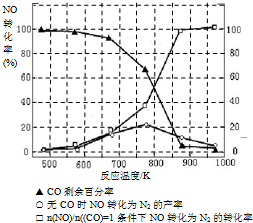
(5)某研究小组在实验室以“Ag-ZSM-5”为催化剂,测得将NO转化为N2的转化率随温度变化情况如下图.据图分析,若不使用CO,温度超过775℃,发现NO的转化率降低,其可能的原因为 ;在
=1的条件下,应控制的最佳温度在 左右.

(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g)?CO2(g)+H2(g).t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气.反应建立平衡后,体系中c(H2)=0.12mol?L-1.则该温度下此反应的平衡常数K=
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(4)用氨气氧化可以生产硝酸,但尾气中的NOx会污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(5)某研究小组在实验室以“Ag-ZSM-5”为催化剂,测得将NO转化为N2的转化率随温度变化情况如下图.据图分析,若不使用CO,温度超过775℃,发现NO的转化率降低,其可能的原因为
| n(NO) |
| n(CO) |

下列有关合成氨的叙述中,正确的是( )
| A、合成氨是天然固氮的一种方法 | B、合成塔是合成氨的关键设备 | C、采用“高温、高压、催化剂”的反应条件,可使N2和H2完全转化为NH3 | D、压强一定时,升高温度可以提高平衡混合物中氨的含量 |
工业上利用合成氨实现人工固氮.属于合成氨主要原料的是( )
| A、NO2 | B、空气 | C、Na2CO3 | D、KNO3 |
符合目前工业生产实际的化工生产原理是( )
| A、合成氨工业中,由于氨易液化,N2、H2循环使用,所以总体上氨的产率很高 | B、氯气和氢气混合在光照条件下反应生成氯化氢,用水吸收得到盐酸 | C、氯碱工业中,电解槽的阳极区产生NaOH | D、二氧化硫在接触室被氧化成三氧化硫,三氧化硫在吸收塔内被水吸收制成浓硫酸 |
接触法制硫酸的生产工艺中,各阶段主要设备的名称正确的是( )
| A、硫磺或硫铁矿的燃烧-沸腾焙烧炉 | B、二氧化硫的催化氧化-氧化炉 | C、三氧化硫的吸收-接触室 | D、将高温炉气进行冷却、除尘和酸洗-吸收塔 |
接触法制硫酸的生产过程中焙烧硫铁矿(含FeS2)时发生的主要化学反应是( )
A、FeS2
| ||||
B、4FeS2+11O2
| ||||
C、4FeS2+15O2
| ||||
D、4FeS2+3O2
|
下列有关工业生产的叙述中正确的是( )
| A、硫酸生产中常采用高压条件来提高SO2的转化率 | B、合成氨中及时分离液态氨来提高化学反应速率 | C、电解精炼铜时,电解液中c(Cu2+)基本保持不变 | D、氯碱工业中阳极得到氢氧化钠和氢气 |
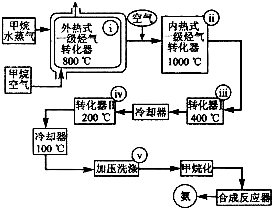 某工厂以天然气、水蒸气和空气为原料和能源合成氨的流程如图.该流程中外热式一级烃转化器系指以CH4为燃料在烃气转化器外面加热使之维持800℃高温的工业装置.内热式一级烃气转 化器系指以H2在装置内燃烧为能量维护一 级烃气转化器所生成的CO与H20(g)反应 生成C02和H2所需1000℃高温的装置.
某工厂以天然气、水蒸气和空气为原料和能源合成氨的流程如图.该流程中外热式一级烃转化器系指以CH4为燃料在烃气转化器外面加热使之维持800℃高温的工业装置.内热式一级烃气转 化器系指以H2在装置内燃烧为能量维护一 级烃气转化器所生成的CO与H20(g)反应 生成C02和H2所需1000℃高温的装置.