 氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.
氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化.(1)对反应2NO2(g)?N2O4(g)△H=-57.2kJ?mol-1
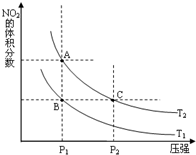
①在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1
②A、C两点气体的平均相对分子质量:A
(2)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②该条件下平衡常数K的值为
③若其他条件不变,下列既能加快正反应速率又能提高NO2转化率的措施是
④若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始的物质的量是
⑤若其它条件不变,只将容器改为带活塞的恒压容器,则平衡时N2O4的量
下列说法正确的是( )
| A、二氧化氮中混有一氧化氮杂质,可通入氧气将一氧化氮转化为二氧化氮 | B、一氧化氮中混有二氧化氮杂质,可将该气体通入水中除去二氧化氮 | C、工业合成氨中的原料氮气和氢气能全部转化为氨气 | D、除去氮气中的少量二氧化碳和水蒸气,可将气体通过盛有NaOH溶液的洗气瓶 |
常见的污染物分为一次污染物和二次污染物.二次污染物是排入环境中的一次污染物在物理、化学因素或微生物作用下,发生变化所生成的新污染物.如反应2NO+O2═2NO2中,二氧化氮为二次污染物.下列三种气体:①二氧化硫;②二氧化氮;③硫化氢,其中能生成二次污染物的是( )
| A、只有①② | B、只有②③ | C、只有①③ | D、全部都是 |
40mLNO、O2混合气体通入到足量的NaOH溶液中充分反应后,溶液中只有NaNO2和NaOH,若剩余气体5mL,则原混合气体中的NO体积为( )
| A、20mL | B、25mL | C、28mL | D、33mL |
下列说法正确的是( )
| A、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | B、检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清夜于试管中,滴加KSCN溶液2-3滴即可 | C、在粗硅的制取中,C+SiO2═Si+2CO 硅被还原,所以碳的还原性大于硅的还原性 | D、用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2 |
标准状况下,将NO2、NO、O2 混合并充满容器,然后把容器倒置于水槽中,充分反应后,水充满容器,则容器中HNO3溶液的物质的量的浓度(mol/L)用M表示范围是( )
A、
| ||||
B、
| ||||
C、
| ||||
D、0<M<
|
最新的病毒学研究证实,一氧化氮对SARS病毒有直接的抑制作用.下列关于一氧化氮的叙述正确的是( )
| A、一氧化氮是红棕色的气体 | B、常温常压下一氧化氮不能与氧气直接化合 | C、一氧化氮不能用排水法收集 | D、氮气和氧气在放电条件下直接得到一氧化氮 |
 硝酸铵是含氮量较高的化肥,生产流程如图(产物水均已略去):
硝酸铵是含氮量较高的化肥,生产流程如图(产物水均已略去):