把铁、氧化铁、氧化铜的混合物粉末放入110mL 4mol?L-1盐酸中,充分反应后产生896mL H2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.4mol?L-1.则原混合物的总质量为( )
| A、14.4 g | B、16 g | C、l2.8 g | D、13.6 g |
有6.4g CuO、Fe2O3混合物跟足量CO充分反应后固体减少了1.44g,反应后全部气体用0.7mol/L Ba(OH)2溶液100mL吸收.下列有关叙述中正确的是( )
| A、反应中生成的CO2体积为2.016 L | B、吸收CO2后的溶液中一定有Ba(HCO3)2 | C、不能确定原混合物中CuO与Fe2O3质量比 | D、若将质量相同的混合物加过量硝酸溶解后,再加入100mL的NaOH溶液时沉淀达最大量,由此可求得c(NaOH)=1.8mol/L |
将质量为W1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,溶液澄清,共收集到标准状况下的气体V1 L.向溶液中逐滴加入浓度为a mol/L的盐酸,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加盐酸体积为V2 L,测得溶液中含盐酸盐溶质共W2 g.下列所列关系式中正确的是( )
| A、35.5a=(W2-W1)V2 | ||
B、n(Na)+3n(Al)=
| ||
C、n(Al)>
| ||
D、aV2=
|
CuO和Fe2O3的混合物m g,向其中加入1mol?L-1的HNO3溶液200mL恰好完全反应,若将m g该混合物用足量CO还原,充分反应后剩余固体质量为( )
| A、(m-3.2)g | B、(2m-3.2)g | C、(m-1.6)g | D、(2m-1.6)g |
将含O2和CH4的混合气体充入有23.4g Na2O2的密闭容器中,电火花点燃,反应结束后,容器内于150℃时压强约为0.将残留物溶于水,无气体逸出.下列叙述正确的是( )
| A、原混合气体中O2和CH4体积比为2:1 | B、原混合气体中O2和CH4体积比为1:2 | C、残留固体中只有Na2CO3 | D、残留固体中只有Na2CO3和NaOH |
常温常压下,往某密闭容器中充入两种气体后不久,测得容器内最终气体平均摩尔质量为49,则充入的气体可能为( )
| A、C2H2和HCl | B、SO2和H2S | C、NH3和HCl | D、NO和O2 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,如图所示流程处理,下列说法中,正确的是( )
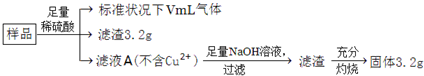
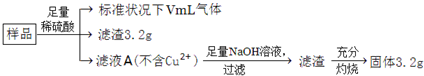
| A、滤液A中阳离子为Fe2+、H+ | B、样品中金属Fe的质量为2.24g | C、样品中CuO的质量为4.0g | D、V=448 |
Na2O2、HCl、Al2O3三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl-、OH-,且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为( )
| A、2:4:1 | B、3:2:1 | C、2:3:1 | D、4:2:1 |
a g Mg、Al合金完全溶解在C1 mol?L-1、V1L HCl溶液中,产生b g H2.再向反应后的溶液中加入C2mol?L-1、V2L NaOH溶液,恰好使沉淀达到最大值,且沉淀质量为d g.下列关系错误的是( )
| A、d=a+17b | ||
B、C1=
| ||
C、铝为
| ||
| D、与金属反应后剩余盐酸为(C1V1-b)mol |
 某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如图所示.当加入1.5mol铁粉并充分反应后的溶液中Fe(NO3)3、Fe(NO3)2、Cu(NO3)2物质的量浓度之比为( )
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如图所示.当加入1.5mol铁粉并充分反应后的溶液中Fe(NO3)3、Fe(NO3)2、Cu(NO3)2物质的量浓度之比为( )| A、1:1:1 | B、1:3:1 | C、2:3:2 | D、1:1:4 |