PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3:2,则剩余固体的组成及物质的量比是( )
| A、1:1混合的Pb3O4、PbO | B、1:2混合的PbO2、Pb3O4 | C、1:4:1混合的PbO2、Pb3O4、PbO | D、1:1:4混合的PbO2、Pb3O4、PbO |
向300mLKOH溶液中缓慢通入一定量的CO2气体,充分反应后,在减压低温下蒸发溶液,得到白色固体.请回答下列问题:(直接填空,不写过程)
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试写出所有可能的组成,填入下表,可以不填满.
(2)若通入CO2气体为2.24L(标准状况下),得到11.9g 的白色固体.请通过计算确定此白色固体组成的物质是 ;所用的KOH溶液的物质的量浓度为 mol/L.
(1)由于CO2通入量不同,所得到的白色固体的组成也不同,试写出所有可能的组成,填入下表,可以不填满.
| 可能情况 | ① | ② | ③ | ④ | ⑤ |
| 组成物质 |
现有2mol/L盐酸和稀硫酸溶液各100mL,分别加入等量的铁粉,反应结束后所生成的氢气体积比为2:3,则加入的铁粉的质量为( )
| A、5.6g | B、8.4g | C、2.8g | D、16.8g |
下列各组物质按如图所示转化关系每一步都能一步实现的是( )
| 甲 | 乙 | 丙 | 丁 |  | |
| A | S | H2S | SO3 | H2SO4 | |
| B | Cu | CuO | CuSO4 | CuCl2 | |
| C | NO | HNO3 | NO2 | NH3 | |
| D | Si | Na2SiO3 | SiO2 | SiF4 |
| A、A | B、B | C、C | D、D |
A~G各物质间的关系如图所示,其中B、D为气体单质.则下列说法错误的是( )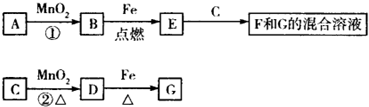

| A、若反应①在常温下进行,则1 mol A在反应中能转移1 mol电子 | ||||
B、反应②的离子方程式为MnO2+4H++2Cl-
| ||||
| C、新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解 | ||||
| D、已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强 |
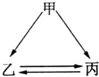 如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是( )①C ②H2O2 ③Na ④Fe ⑤HNO3.
| A、仅①③④ | B、仅①②⑤ | C、仅①②③⑤ | D、①②③④⑤ |
根据下列框图,有关说法正确的是( )
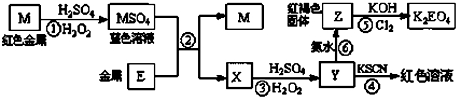

| A、M、E都是第四周期中的过渡元素,E的金属活动性比M的金属活动性强,E3+的氧化性比M2+的氧化性弱 | B、反应⑤的离子方程式可表示为:2E(OH)3+3Cl2+6H2O═3EO42-+6Cl-+12H+ | C、反应①、②、③、⑤都属于氧化还原反应,且在反应①和③中硫酸仅表现了酸性 | D、用K2EO4、Zn可制成一种高能电池,该电池中负极的电极反应式为:EO42-+4H2O+3e-═E(OH)3+5OH- |
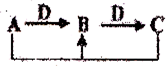 A、B、C、D是中学化学常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )
A、B、C、D是中学化学常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化关系如图,下列判断正确的是( )| A、若D为H2O,A为碳,则A和C反应生成1 mol B转移的电子数为NA | ||
| B、若D为Fe,A为CI2,则B溶液蒸干后可得到纯净的B固体 | ||
| C、若D为O2,A为碱性气体,则以上转化只涉及两个氧化还原反应 | ||
D、若D为HCl,A为Na2CO3,则B溶液中c(Na+)=c(HCO3-)+2c(CO
|
 下列各组物质中,不是按如图 (“→”表示一步完成)关系相互转化的是( )
下列各组物质中,不是按如图 (“→”表示一步完成)关系相互转化的是( ) Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如通常所说的“铁三角”、“铝三角”等.下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )
Na、Al、Fe、Cu是中学化学中重要的金属元素,它们的单质及其化合物之间有很多转化关系,如通常所说的“铁三角”、“铝三角”等.下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是( )