 甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是( )
甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是( )| A、若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3 | ||||
B、若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式4NH3+5O2
| ||||
| C、若甲、乙、丙的溶液显碱性,丙可作为医疗上治疗胃酸过多症的药剂,将等物质的量的乙和丙溶于水形成混合溶液,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | ||||
| D、若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐 |
 元素X的单质及X与元素Y形成的化合物存在如图所示的关系(其中m≠n,且均为正整数).下列说法正确的是( )
元素X的单质及X与元素Y形成的化合物存在如图所示的关系(其中m≠n,且均为正整数).下列说法正确的是( )| A、X一定是金属元素 | B、(n-m)一定等于1 | C、由X生成1mol XYm时转移的电子数目一定为4NA | D、三个化合反应一定都是氧化还原反应 |
 已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )
已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )| A、甲为C,X为O2 | B、甲为SO2,X为NaOH溶液 | C、甲为Fe,X为Cl2 | D、甲为AlCl3,X为NaOH溶液 |
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物.“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物.该药品不溶于水但能溶于人体中的胃酸.某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验: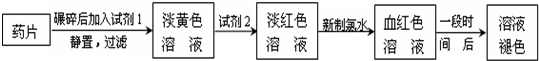
(1)试剂1是 .
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 .
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去.为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确.写出有关的实验操作、预期现象和结论.(不一定填满,也可以补充)

(1)试剂1是
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去.为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
| 编号 | 猜想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 编号 | 实验操作 | 预期现象和结论 |
为证明化学反应有一定的限度,进行如下探究活动:
I.取5ml 0.1mol/L的KI溶液,滴加5-6滴FeCl3稀溶液;
Ⅱ.继续加入2mlCCl4振荡
Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为 .
探究活动Ⅱ的实验现象为 .
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高.
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
②写出实验操作“步骤一”中的反应离子方程式: .
Ⅳ.为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作:
①移取25.00mLFeCl3稀溶液至锥形瓶中,加入 用作指示剂,再用c mol/LKI标准溶液滴定,达到滴定终点时的现象是 .
②重复滴定三次,平均耗用c mol/LKI标准溶液VmL,则FeCl3稀溶液物质的量浓度为 mol/L.
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 (填“偏高”或“偏低”或“不变”).
0 59845 59853 59859 59863 59869 59871 59875 59881 59883 59889 59895 59899 59901 59905 59911 59913 59919 59923 59925 59929 59931 59935 59937 59939 59940 59941 59943 59944 59945 59947 59949 59953 59955 59959 59961 59965 59971 59973 59979 59983 59985 59989 59995 60001 60003 60009 60013 60015 60021 60025 60031 60039 203614
I.取5ml 0.1mol/L的KI溶液,滴加5-6滴FeCl3稀溶液;
Ⅱ.继续加入2mlCCl4振荡
Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为
探究活动Ⅱ的实验现象为
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高.
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
| 实验操作 | 现象和结论 |
| 步骤一: | 若产生蓝色沉淀,则 |
| 步骤二: | 若乙醚层呈血红色,则 |
Ⅳ.为了测定探究活动I中的FeCl3稀溶液的浓度,现进行以下操作:
①移取25.00mLFeCl3稀溶液至锥形瓶中,加入
②重复滴定三次,平均耗用c mol/LKI标准溶液VmL,则FeCl3稀溶液物质的量浓度为
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果
