 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着 Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A、a点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ | B、b点消耗Ba(OH)2溶液体积为200mL | C、从a→b、b→c点过程中发生反应的离子方程式依次为:NH4++OH-=NH3?H2O Al(OH)3+OH-=AlO2-+2H2O | D、沉淀的质量:a点>c点 |
Fe2O3和Al2O3都( )
| A、是两性氧化物 | B、可与氢氧化钠溶液反应 | C、可与盐酸反应 | D、可溶于水 |
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述正确的是( )
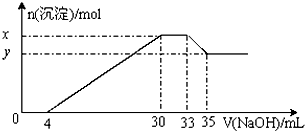

| A、原溶液中n(Mg2+):n(Al3+)=10:1 | B、原溶液中的c(H+)=0.8mol/L | C、x与y的差值为0.01mol | D、原溶液中c(Cl-)=0.66mol/L |
实验室中,要使AlCl3溶液中的Al3+离子全部沉淀出来,适宜用的试剂是( )
| A、NaOH溶液 | B、Ba(OH)2溶液 | C、盐酸 | D、氨水 |
下列物质的转化在给定条件下不能实现的是( )
A、Al2O3
| |||||
B、SiO2
| |||||
C、HCl
| |||||
D、Fe
|
向10mL 2mol/L的氯化铝溶液中加入0.5mol/L的烧碱溶液,反应得到沉淀0.78g,则加入的烧碱溶液的体积可能为( )
| A、30mL | B、60mL | C、90mL | D、140mL |
向MgSO4、Al2(SO4)3、(NH4)2SO4的混合液中,逐滴加入NaOH溶液,下列图象中,能正确表示上述反应的是(横坐标表示加入NaOH溶液的体积,纵坐标表示生成沉淀的质量)( )
A、 | B、 | C、 | D、 |
以下物质间的每步转化通过一步反应能实现的是( )
①Al→Al2O3→Al(OH)3
②Fe→FeCl3→Fe(OH)3
③Si→SiO2→H2SiO3
④N2→NO→NO2.
①Al→Al2O3→Al(OH)3
②Fe→FeCl3→Fe(OH)3
③Si→SiO2→H2SiO3
④N2→NO→NO2.
| A、①② | B、③④ | C、①③ | D、②④ |







