已知反应:Na2O2+SO2=Na2SO4,则下列判断正确的是( )
| A、硫元素被还原 | B、二氧化硫是还原剂 | C、过氧化钠既是氧化剂又是还原剂 | D、二氧化硫既不是氧化剂也不是还原剂 |
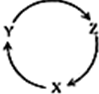 下表中各组物质,不能满足如图物质一步转化关系的选项是( )
下表中各组物质,不能满足如图物质一步转化关系的选项是( )| X | Y | Z | |
| A | NaCl | Na2CO3 | NaHCO3 |
| B | C2H5OH | CH2=CH2 | C2H5Br |
| C | AlCl3 | Al(OH)3 | NaAlO2 |
| D | NO | NO2 | HNO3 |
| A、A | B、B | C、C | D、D |
下列各组物质混合后,不能生成NaOH的是( )
| A、Na2O和H2O | B、Na2O2和H2O | C、Ca(OH)2溶液和Na2CO3溶液 | D、Ca(OH)2溶液和NaCl溶液 |
下列叙述不正确的是( )
| A、含金属元素的离子一定是阳离子 | B、应用蒸馏的方法,可以分离沸点相差较大的液体混合物 | C、氯水和过氧化钠都具有漂白作用,其漂白原理相似 | D、高炉炼铁时,还原铁矿石的还原剂为一氧化碳 |
将15.6gNa2O2和5.4gAl同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则下列说法正确的是( )
| A、标准状况下,反应过程中得到8.96L气体 | B、最终得到的溶液中:c(Na+)=c(Cl-)+c(OH-) | C、最终得到5.6g沉淀 | D、最终得到的溶液中:c(Na+)=1.5mol?L-1 |
为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了以下四种不同的方案,其中方法和现象判断不正确的是( )
| A、用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色 | B、分别取样配成溶液,滴加CaCl2溶液,观察有无白色沉淀 | C、分别加入1mol/L的盐酸溶液,看有无气泡产生 | D、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
下列各实验中,先产生沉淀,然后沉淀又溶解的是( )
①向饱和碳酸钠溶液中通入CO2至过量
②向氯化铝溶液中逐滴加入氢氧化钠溶液至过量
③向AgNO3溶液中逐滴加入氨水至过量
④向硅酸钠溶液中逐滴加入盐酸至过量.
①向饱和碳酸钠溶液中通入CO2至过量
②向氯化铝溶液中逐滴加入氢氧化钠溶液至过量
③向AgNO3溶液中逐滴加入氨水至过量
④向硅酸钠溶液中逐滴加入盐酸至过量.
| A、①② | B、①③ | C、①④ | D、②③ |
下列关于物质的用途叙述不正确的是( )
| A、过氧化钠可用作供氧剂 | B、高纯硅用来制造光导纤维 | C、镁铝合金可用作制造飞机的材料 | D、Cl2可与石灰乳反应制取漂白粉 |
下列说法正确的是( )
| A、Na2CO3比NaHCO3的溶解度小 | B、质量相同的Na2CO3和NaHCO3与足量盐酸反应可生成等量的CO2 | C、石灰水可鉴别Na2CO3和NaHCO3溶液 | D、Na2CO3和NaHCO3同时与质量分数相等.质量相等的盐酸反应,后者放出气体快 |
下列四组反应中既有白色沉淀产生,又有气体放出的是( )
| A、Na2O2和CuSO4溶液反应 | B、金属钠投入到MgSO4溶液中 | C、BaCl2和NaHSO4溶液反应 | D、纯碱溶液和澄清石灰水反应 |