配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
| A、所用NaOH已经潮解 | B、向容量瓶中加水未到刻度线 | C、摇匀后,液面低于刻度线,再加水至刻度线 | D、定容时,仰视刻度线 |
为达到预期的实验目的,下列操作正确的是( )
| A、欲配制质量分数为10%的ZnSO4溶液,将10gZnSO4.7H2O 溶解在90g水中 | B、欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 | C、欲配制0.2mol/L的Na2CO3溶液950mL,需要称量Na2CO3固体21.2g | D、欲配制0.1mol/L的NaOH溶液,将4.0g NaOH溶解于lL水中 |
配制0.1mol/L的NaCl溶液,下列操作会导致所配溶液浓度偏低的是( )
| A、称量时,右盘高,左盘低? | B、定容时俯视读取刻度? | C、原容量瓶洗净后未干燥? | D、定容时液面超过了刻度线? |
利用100mL0.50mol?L-1 Na2CO3溶液配制Na+浓度为0.20mol?L-1的溶液,下列操作正确的是( )
| A、将该Na2CO3溶液转移至250mL容量瓶中,加蒸馏水稀释至刻度线,摇匀 | B、将该Na2CO3溶液转移至250mL烧杯中,用量筒量取150mL蒸馏水加入,搅拌 | C、将该Na2CO3溶液转移至500mL烧杯中,用量筒量取400mL蒸馏水加入,搅拌 | D、将该Na2CO3溶液转移至500mL容量瓶中,加蒸馏水稀释至刻度线,摇匀 |
配置250mL 0.100mol/L的氯化钠溶液,操作不正确的是( )
A、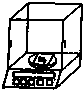 称量 | B、 溶解 | C、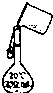 转移 | D、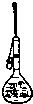 定容 |
配制一定物质的量浓度的溶液,一定不需要的仪器是( )
①蒸馏烧瓶 ②容量瓶 ③玻璃棒 ④量筒 ⑤烧杯.
①蒸馏烧瓶 ②容量瓶 ③玻璃棒 ④量筒 ⑤烧杯.
| A、①③ | B、②⑤ | C、① | D、④⑤ |
甲、乙、丙三位同学进行下列实验:各取30.0mL同浓度的盐酸(密度:1.01g/ml),分别加入相同的镁铝合金进行反应,收集生成的气体,各记录有关数据如下:
试计算:
(1)盐酸溶液的质量分数;
(2)合金中镁铝的质量比.
0 59580 59588 59594 59598 59604 59606 59610 59616 59618 59624 59630 59634 59636 59640 59646 59648 59654 59658 59660 59664 59666 59670 59672 59674 59675 59676 59678 59679 59680 59682 59684 59688 59690 59694 59696 59700 59706 59708 59714 59718 59720 59724 59730 59736 59738 59744 59748 59750 59756 59760 59766 59774 203614
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(g) | 0.255 | 0.385 | 0.495 |
| 气体质量(g) | 0.025 | 0.030 | 0.030 |
(1)盐酸溶液的质量分数;
(2)合金中镁铝的质量比.