我国规定饮用水质量标准必须符合下列要求
| pH | 6.5~8.5 |
| Ca2+、Mg2+总浓度 | <0.0045mol·L-1 |
| 细菌总数 | <100个/mL |
 曝气池
曝气池 一级沉降池
一级沉降池 二级沉降池
二级沉降池 过滤池
过滤池 自来水
自来水(1)FeSO4·7H2O是常用的凝聚剂,它在水中最终生成__________
(2)气体A的作用是。这种作用是基于(气体A和水反应的产物具有__________性。
(3)下列物质中可以作为气体A的代用品_________(填写编号)。
①Ca(ClO)2 ②NH3(液)③K2FeO4④SO2
自来水厂的水源水(原水)通常含有各种杂质,必须经过去除固体杂质和悬浮物、消毒、去除异味等一系列净化工序(即净化过程),才能达到使用标准。
(1)原水净化有下列措施:①过滤,②添加混凝剂,③加入活性炭,④加入消毒剂。你认为正确的顺序是 ;
| A.①②③④ | B.②①③④ | C.②③①④ | D.④①②③ |
(3)目前我国不少自来水厂采用液氯消毒,液氯注入水中与水发生可逆反应,生成一种强酸和一种弱酸(次氯酸),该反应的化学方程式为______________________________。
(1)有人研究证明:使用氯气作自来水消毒剂,氯气会与水中有机物反应,生成如CHCl3等物质,这些物质可能是潜在的致癌致畸物质。目前人们已研发多种饮用水的新型消毒剂。下列物质不能作自来水消毒剂的是 (填序号)。
| A.硫酸铜 | B.二氧化氯 | C.臭氧 | D.硫酸亚铁 |
。
(3)用高铁(VI)酸盐设计的高铁(VI)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应:3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(O
 H)3+4KOH
H)3+4KOH①写出正极发生的电极反应式: 。
②用高铁(VI)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2molK2FeO4反应时,则在电解池中生成H2 L(标准状况)。
③
 下表列出了某厂排放
下表列出了某厂排放 的含锌废水中的含量及国家环保标准值的有关数据:
的含锌废水中的含量及国家环保标准值的有关数据:| | 某厂含锌废水水质 | 国家环保标准值 |
| Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
| pH | 1~5 | 6~9 |
 (填“符合”或“不符合”)国家环保标准。(常温下,Ksp[Zn(OH)2]=1.2×10-17)
(填“符合”或“不符合”)国家环保标准。(常温下,Ksp[Zn(OH)2]=1.2×10-17) 绿色化学的核心就是利用化学原理从源头上减少和清除工业生产对环境的污染。按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,这时原子的利用率为 。 是甲基丙烯酸甲酯的结构简式。也可以写成CH2 = C(CH3)COOCH3。
是甲基丙烯酸甲酯的结构简式。也可以写成CH2 = C(CH3)COOCH3。
旧法合成它的反应是:
(CH3)2C = O+HCN (CH3)2C(OH)CN
(CH3)2C(OH)CN
(CH3)2C(OH)CN + CH3OH + H2SO4  CH2 = C(CH3)COOCH3+NH4HSO4
CH2 = C(CH3)COOCH3+NH4HSO4
新法合成它的反应是:
CH3C ≡ CH + CO + CH3OH  CH2= C(CH3)COOCH3
CH2= C(CH3)COOCH3
(1)与旧法相比,新法的突出优点是( )
| A.原料无爆炸危险 | B.原料都是无毒物质 |
| C.没有副产物,原子利用率高 | D.对设备腐蚀性小 |
(原子利用率=期望产物的总质量与生成物的总质量之比)
(3)写出聚甲基丙烯酸甲酯(又称有机玻璃)的结构简式 。
(本题共15分)空气中CO2浓度的持续走高引起人们的高度重视。一些科学家认为,人类不仅要努力减少CO2的排放,还要尽快想办法清除空气中过多的CO2。为此,他们设想了一系列“捕捉”和“封存” CO2的方法。
【小题1】方法Ⅰ:一些科学家利用太阳能加热的反应器“捕捉”空气中的CO2,如下图所示。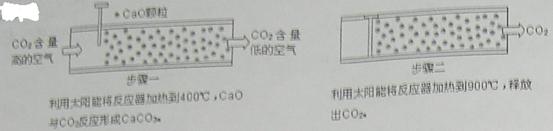
(1)步骤一中的CaO俗称 。
(2)步骤二中发生反应的化学方程式是 ,该反应 (填“是”或“不是”)步骤一中反应的逆反应。
【小题2】方法Ⅱ:另一些科学家利用NaOH溶液的喷淋“捕捉”空气中的CO2,如右图所示。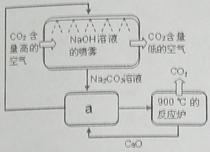
(1)NaOH溶液喷成雾状是为了 。
(2)右图a环节中,物质分离的基本操作是 。
(3)为了尽量减少成本,在整个流程中,循环利用的物质有CaO和 。
【小题3】下列溶液中,同样能用于“捕捉”二氧化碳的是( )。
| A.KNO3溶液 | B.CaCl2溶液 | C.CuSO4溶液 | D.Na2CO3溶液 |
①方法Ⅰ将受到地域的限制
②方法Ⅱ的能耗太大
③方法Ⅰ中使用的是氧化钙颗粒而不是氧化钙粉末
④方法Ⅱ中的物质可以循环利用,但方法Ⅰ中的却不能
| A.①③ | B.①② | C.②④ | D.③④ |
可见,要真正实现“碳捕捉”和“碳封存”的设想,科学家任重而道远。
 下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl- 、Ca2+、Mg2+、
下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl- 、Ca2+、Mg2+、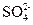 等离子,电极为惰性电极。请分析下列问题:
等离子,电极为惰性电极。请分析下列问题: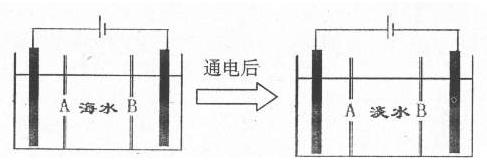

 Ⅴ中NaHCO3gm V
Ⅴ中NaHCO3gm V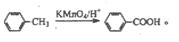
 )的合成路线流程图(必要条件需注明,无机试剂任选)。合成路线流程图示例如下:
)的合成路线流程图(必要条件需注明,无机试剂任选)。合成路线流程图示例如下: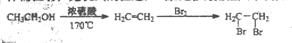
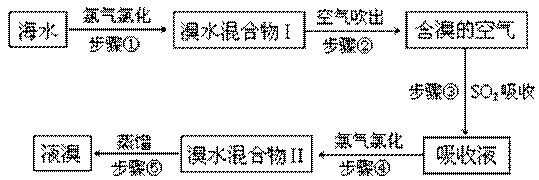
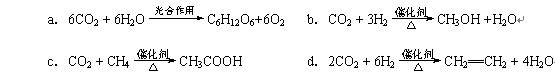 以上反应中,最节能的是 ,原子利用率最高的是 。
以上反应中,最节能的是 ,原子利用率最高的是 。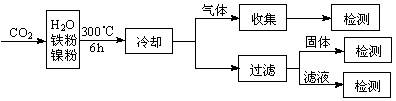
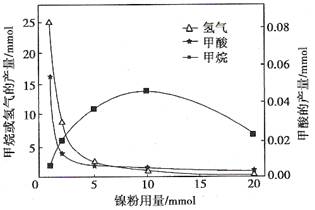
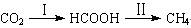
 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1