工业制硫酸铜不是直接用铜和浓硫酸反应,而是将粗铜(含少量银)浸入稀硫酸中,并不断从容器下部吹入细小的空气泡。有关该制备方法的叙述中,正确的是( )
(1)该方法应用了原电池工作原理 (2)该方法应用了电解池工作原理
(3)该方法不产生污染大气的二氧化硫 (4)该方法提高了硫酸的利用率
(5)该方法提高了铜的利用率
| A.(1)(3)(5) | B.(2)(3)(4) | C.(1)(3)(4) | D.(1)(3)(4)(5) |
1913年德国化学家哈伯发明了以低成本制造大量氨的方法,从而大大满足了当时日益增长的人口对粮食的需求。下列是哈伯法的流程图,其中为提高原料转化率而采取的措施是( )。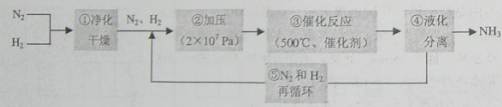
| A.①②③ | B.②④⑤ | C.①③⑤ | D.②③④ |
下列有关工业生产的叙述正确的是
| A.用明矾净水是因为Al3+水解生成Al(OH)3胶粒具有很强的吸附性 |
| B.合成氨生成过程中,采用高温高压都是为了提高N2、H2转化率 |
| C.硫酸工业中,在接触室安装热交换器是为了利用硫铁矿燃烧时放出的热量 |
| D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
右图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是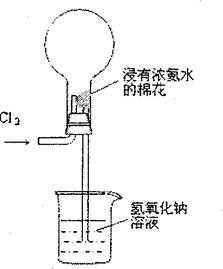

| A.烧瓶中立即出现白烟 |
| B.烧瓶中立即出现红棕色 |
| C.烧瓶中发生的反应表明常温下氨气有还原性 |
| D.烧杯中的溶液是为了吸收有害气体 |
下列过程合乎实际并用于工业生产的是( )
| A.钠在氯气中燃烧制氯化钠 | B.氯化铵与氢氧化钙共热制氨气 |
| C.浓盐酸与二氧化锰共热制氯气 | D.氯气与石灰乳反应制漂白粉 |
合成氨工业对国民经济和社会发展具有重要的意义。哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%;最近美国俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)2的催化剂,在常温下合成出氨。下列有关说法中错误的是
| A.新的催化剂降低了反应所需要的能量 |
| B.新法合成和哈伯法相比不需要在高温条件下,可节约大量能源 |
| C.新法合成能在常温下进行是因为催化剂降低了反应的活化能 |
| D.哈伯法合成氨是吸热反应,新法合成氨是放热反应 |
下列工业生产的说法错误的是
| A.氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产方法又称“阳离子交换膜法” |
| B.生产普通玻璃的主要原料及设备:石灰石、石英、纯碱及玻璃熔炉 |
| C.由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件 |
| D.合成氨的反应是放热反应,因此工业合成常采用低温条件 |
下列叙述正确的是
| A.合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率 |
| B.硫酸工业中,接触室中热交换器是利用SO3转化为H2SO4时放出的热量 |
| C.氯碱工业采用离子交换膜法,可防止阳极室产生的Cl2进入阴极室 |
| D.钢铁发生吸氧腐蚀时,阴极的反应式为:Fe-2e→Fe2+ |
下列化工生产过程中不涉及氧化还原反应的是
| A.氯碱工业 | B.硫酸工业 | C.玻璃工业 | D.合成氨工业 |
合成氨反应:N2(g) + 3H2(g)  2NH3(g) ,在反应过程中,
2NH3(g) ,在反应过程中, t1、t2、t3、t4时条件改变,正反应速率发生变化,如右图,对于可能的条件改变下列判断正确的是
t1、t2、t3、t4时条件改变,正反应速率发生变化,如右图,对于可能的条件改变下列判断正确的是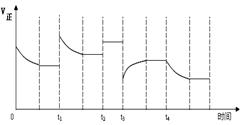
A.t1时可能升高了温度 | B.t2时可能使用了催化剂 |
C.t3时可能减小了压强 | D.t4时可能降低了温度 |