(14分)三苯甲醇( )是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
)是重要的有机合成中间体,实验室中合成三苯甲醇时采用图2所示的装置,其合成流程如图1所示。
图1
已知:(1)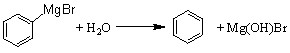 (碱式溴化镁);
(碱式溴化镁);
(2)相关物质的物理性质如下:
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | -30.7°C | 156.2°C | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸乙酯 | -34.6°C | 212.6°C | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,不溶于醇、醚等有机溶剂 | |
(1)写出装置图中玻璃仪器的名称:A ,导管B的作用 ;
(2)制取格氏试剂时要保持微沸,可以采用水浴加热,优点是 ,微沸回流时冷凝管中水流的方向是
(填“X→Y”或“Y→X”),装有无水CaCl2的仪器A的作用是 ;
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下提纯方案,请填写空白:

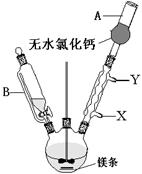
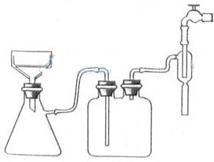
图2 图3
(4)抽滤时所用装置如图3所示,该装置存在的错误有 ,抽滤完毕或中途停止抽滤时的操作方法:应先 ,然后 ;
(5)洗涤液最好选用 ,检验产品已经洗涤干净的操作为 。
(A)水(B)乙醚 (C)乙醇 (D)苯
(9分)某校一化学实验小组通过实验分析,确定一红色粉末为Fe2O3和Cu2O的混合物。
己知:①Cu2O溶于稀硫酸生成Cu和CuSO4,②Cu2O在空气中加热生成CuO。
(1)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为__________。
(2)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | 供选择试剂 |
| Fe3+ | 1.9 | 3.7 | A.氯水, B.H2O2, C.NaOH, D.氨水, E.CuO, F.Cu2(OH)2CO3 |
| Fe2+ | 7.5 | 11 | |
| Cu2+ | 6.0 | 10 |
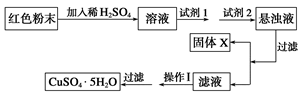
试回答:
①试剂1可以为________________,试剂2可以为________________。
②固体X的化学式为____________。
③操作Ⅰ为____________________。
(14分)某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)实验室中现有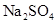 、
、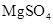 、
、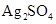 、
、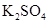 等4中溶液,可与实验中
等4中溶液,可与实验中 溶液起相似作用的是 ;
溶液起相似作用的是 ;
(4)要加快上述实验中气体产生的速率,还可采取的措施有 (答两种);
|
|
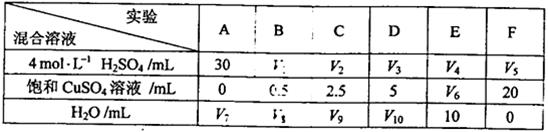
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②实验E中的金属呈 色;
③该同学最后得出的结论为:当加入少量
 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因 。 (14分)某同学探究同周期元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
| 实验步骤 | 实验现象 |
| ①将一小块金属钠放入滴有酚酞的冷水中 | A.剧烈反应,产生大量无色气体。 |
| ②将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加酚酞溶液 | B.浮在水面,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ③将镁条放入稀盐酸中 | C.生成淡黄色沉淀。 |
| ④将铝条放入稀盐酸中 | D.反应较快,产生无色气体。 |
| ⑤向AlCl3溶液中滴加NaOH 溶液至过量 | E.有气体产生,溶液变成浅红色。 |
| ⑥向新制的Na2S溶液中滴加新制的氯水 | F.产生白色胶状沉淀,继而沉淀消失。 |
(1)实验目的:研究同周期元素性质递变规律。
(2)实验药品:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH 溶液等。
实验仪器:试管、试管夹、酒精灯、胶头滴管、镊子、小刀、玻璃片、砂纸等。
(3)实验内容(填写与实验步骤对应的实验现象的标号和化学方程式)
| 实验内容 | 实验现象 | 化学方程式 |
| ① | B | |
| ② | | Mg + 2H2O  Mg(OH)2 + 2H2 ↑ Mg(OH)2 + 2H2 ↑ |
| ③ | | Mg + 2HCl = MgCl2 + H2↑ |
| ④ | D | |
| ⑤ | | AlCl3 + 3NaOH = Al(OH)3↓+ 3NaCl Al(OH)3 + NaOH = NaAlO2 + 2H2O |
| ⑥ | | Na2S + Cl2 =" 2NaCl" + S↓ |
(8分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用带刻度的集气瓶排水法收集氢气,每隔1分钟记录一次数据(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
造成这种变化的主要因素是 ;从3~5分钟时间段内,产生氢气的速率是如何变化的?答: 。造成这种变化的主要因素是 。
(2)在盐酸中分别加入等体积的下列溶液,能减缓反应速率而又不减少产生氢气的量的是 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
(3)在0~1、1~2、2~3、3~4、4~5分钟五个时间段中,反应速率最大的时间段的盐酸的反应速率为 (设溶液体积不变,上述气体体积为标况下数据)。

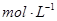 NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为
NaOH溶液中,判断锌层完全反应的标志是:__________,最后,取出铁片用水冲洗、烘干后称量,得质量为m2,设锌镀层单侧厚度为h,锌的密度为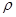 ,则h=__________
,则h=__________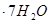 含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有:
含量的步骤是:称1g绿矾,用30mL蒸馏水溶解并加入H2SO4溶液和H3PO4溶液,再用0.02mol/L KMnO4标准溶液滴定到溶液刚变成粉红色,停止滴定,消耗标准溶液VmL。反应中涉及的重要化学方程式有: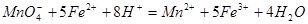
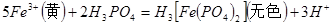
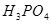 的作用是__________。
的作用是__________。