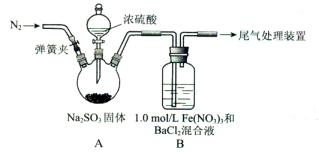
(15分)某课外小组对一些金属单质和化合物的性质进行研究。
(1?)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片?过量?放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色[视其主要成分为 |
| Cu2?OH?2CO3 | |
置换反应____________,
化合反应____________。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是______________________________________________。
解释此现象的离子方程式是_______________。
(3)工业上可用铝与软锰矿?主要成分为MnO2?反应来冶炼金属锰。
①用铝与软锰矿冶炼锰的原理是?用化学方程式表示?_____________________________。
② MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式______________________________。
(7分)某研究小组为了探究甲烷和氯气反应情况,设计了几个实验。请填写下列空白: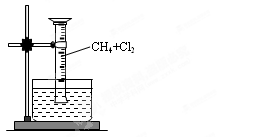
【实验一】用如图所示装置,排水法收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
(1)该反应的化学方程式为 (只写第一步);该反应属于 (填反应类型)
(2)水槽中盛放的液体最好为 ;(填标号)
| A.水 | B.饱和石灰水 | C.饱和食盐水 | D.饱和NaHCO3溶液 |
(3)该实验设计的错误之处 __________________________________ ;(用反应方程式和必要的文字加以说明)
为了研究外界条件对H2O2分解速率的影响,某同学做了以下实验,请回答下列问题。
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5%H2O2溶液,各滴入2滴1 mol/L FeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中。 | 试管A中产生气泡量减少;试管B中产生的气泡量增大。 |
| ② | 另取两支试管分别加入5mL 5%H2O2溶液和5mL 10%H2O2溶液 | 试管A、B中均未明显见到有气泡产生。 |
(2)实验①的目的是________。
(3)实验②未观察到预期的实验现象,为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是_______(用实验中所提供的几种试剂)。
(4)某同学在50 mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如下图所示,则A、B、C三点所表示的瞬时反应速率最快的是______(填“A”或“B”或“C”)。

(5)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

①定性分析:如图甲可通过观察_________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_______。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是_________。
14分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用带刻度的集气瓶排水法收集氢气,每隔1分钟记录一次数据(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
造成这种变化的主要因素是_________________;从3~5分钟时间段内,产生氢气的速率是如何变化的?答:_________。造成这种变化的主要因素是_____________________。
(2)在盐酸中分别加入等体积的下列溶液,能减缓反应速率而又不减少产生氢气的量的是___________(双选题,漏选得1分,多选,错选得0分)。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
(3)在0~1、1~2、2~3、3~4、4~5分钟五个时间段中,反应速率最大的是在____分钟时间段内,在该时间段内盐酸的反应速率为 (设溶液体积不变,上述气体体积为标况下数据)。
(16分)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式,实验用到的仪器如下图所示:
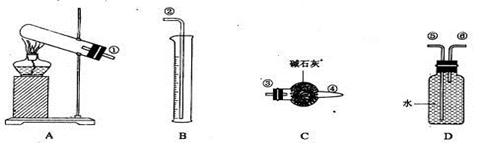 |
【提出猜想】
I.所得气体的成分可能只含_________一种;
II.所得气体的成分可能含有__________二种;
III.所得气体的成分可能含有SO2、SO3、O2三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。
请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,行仪器接口连接顺序为__________(填序号);
(2)若实验结束,B中量筒没有收集到水,则证明猜想__________正确;
(3)实验过程,仪器C的作用是 ________________________;
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
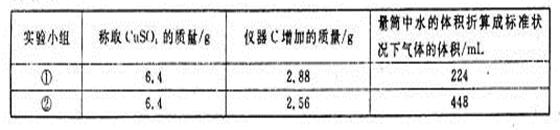
请通过计算,推断出第①小组和第②小组的实验条件下CuSO4分解的化学反应方程式:
① 组_________________________________________________________________;
② 组_______________________________________________________________。

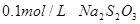 溶液、
溶液、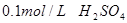 、烧杯、冷水、热水、秒表等
、烧杯、冷水、热水、秒表等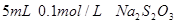 。
。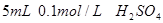 。
。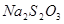 和
和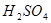 反应的化学方程式为 。
反应的化学方程式为 。