下列关于实验原理或操作的叙述中,正确的 是 ( )
是 ( )
| A.用无水乙醇从碘水中提取单质碘 |
B.稀释浓 硫酸时,应将浓硫酸缓缓注入盛有水的量筒中 硫酸时,应将浓硫酸缓缓注入盛有水的量筒中 |
| C.配制.FeCl3溶液时,向溶液中加入少量Fe和稀盐酸 |
| D.提纯混有少量乙酸的乙醇,可先加生石灰再蒸馏 |
从下列事实所列出的相应结论正确的是 ( )
| | 实 验 事 实 | 结 论 |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| D | SO2通入KMnO4溶液,溶液褪色 | SO2具有漂白性 |
关于实验下列说法错误的是( )
A.在硫酸铜晶体结晶水含量的 测定实验中,加热后的硫酸铜应在空气中冷却后 测定实验中,加热后的硫酸铜应在空气中冷却后 再称量 再称量 |
| B.在中和热的测定实验中,应用稀的强酸和强碱作为反应物进行实验 |
| C.在Fe(OH)3胶体的电泳实验中,靠近阴极附近的液体的颜色会加深 |
| D.在硫酸铜晶体结晶水含量的测定实验中,加热不够充分将会使实验结果偏小 |
在酸性条件下H2C2O4可以被KMnO4溶液氧化,使KMnO4溶液褪色,依据KMnO4溶液褪色时间的长短可以比较反应进行的快慢。下列各组实验中溶液褪色最快的是
| 组号 | 反应温度 /℃ | 参加反应物质 | ||||
| KMnO4 | H2C2O4 | MnSO4 | ||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | m/g | ||
| A | 20 | 4 | 0.1 | 2 | 0.1 | 0 |
| B | 20 | 4 | 0.1 | 2 | 0.1 | 0.1 |
| C | 40 | 4 | 0.1 | 2 | 0.1 | 0 |
| D | 40 | 4 | 0.1 | 2 | 0.2 | 0.1 |
小张用白纸和无色溶液给表弟写了一封“无字”信,表弟接到信拆开一看觉得很愕然,但沉思一下便明白小张的意 思。经过用另一溶液简单处理后,表弟看到了一封有颜色的信,并很快写了回信。小张和表弟所用的溶液分别可能是( )。
思。经过用另一溶液简单处理后,表弟看到了一封有颜色的信,并很快写了回信。小张和表弟所用的溶液分别可能是( )。
A.前者是紫色石蕊试液,后者是稀盐酸 | B.前者是NaOH稀溶液,后者是稀硫酸 |
| C.前者是浓硫酸,后者是紫色石蕊试液 | |
| D.前者是米汤,后者是碘酒 |
下列有关化学研究的正确说法是
| A.化学家提出的假设不一定能被实验证实 |
| B.同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| C.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增的规律 |
| D.科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,标志着化学已成为以理论研究为主的学科,不需要再做化学实验 |
.某研究性学习小组为了探究镁粉与溴水反应的机理,做了如下四种实验:①将镁粉投入到冷水中,未观察到明显现象;②将镁粉投入到溴水中,观察到只是开始时产生极少量的气泡,但溴水会慢慢退色;③将镁粉投入到液溴中,未观察到明显现象;④向含有足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快退去。下列关于镁粉与溴水的反应机理的叙述中正确的是
| A.镁粉只直接与溴水中的溴反应 | B.镁粉只与溴水中的酸反应 |
| C.产生极少量的气泡是由于镁粉与水反应得到的 | D.镁粉在水的催化下与溴发生反应 |
用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是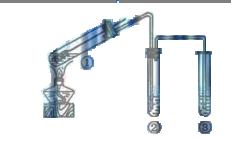
A.上下移动①中铜丝可控制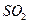 的量 的量 |
B.②中选用品红溶液验证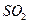 的生成 的生成 |
C.③中选用NaOH溶液吸收多余的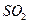 |
D.为确认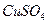 生成,向①中加水,观察颜色 生成,向①中加水,观察颜色 |
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响)。则滴管和烧瓶中所用试剂可能是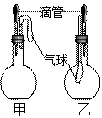
| A.甲:稀硫酸和铜片 乙:浓氨水和SO2 |
| B.甲:双氧水和MnO2 乙:NaOH溶液和CO2 |
| C.甲:NaHCO3溶液和苯酚乙:NaOH溶液和Cl2 |
| D.甲:浓硫酸和蔗糖(滴有几滴水)乙:水和N2 |
