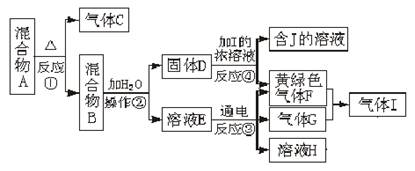
黄铁矿的主要成分是FeS2。测定黄铁矿中FeS2含量的两种方法如下图所示: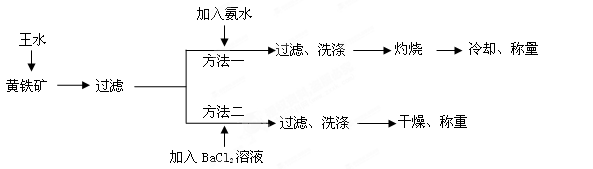
已知:
①王水是由1体积的浓硝酸(ρ=1.42g·cm-3)和3体积的浓盐酸(ρ=1.19g·cm-3)混合而成的。
②黄铁矿和王水反应的方程式为Fe S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
S2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O
请回答下列问题:
(1)简述实验室配制王水的操作过程_____________________________________
(2)方法一中过滤、洗涤、灼烧都用到的仪器是_______________。
(3)方法二中要判断BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是____(填代号)
| A.NaOH | B.BaCl2 | C.HCl | D.Na2SO4 |
试剂:①浓硫酸 ②浓盐酸 ③食盐固体
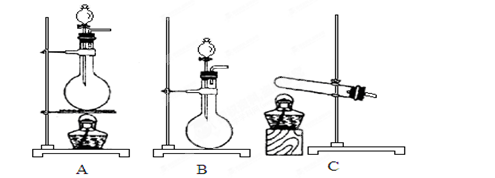
若选用试剂①②,则宜选择的装置是____________。
若选用试剂①③,则应选择的装置是___________(填代号,下同);推测发生反应的化学方程式为__________________________________________________;
(5)方法一中,灼烧时发生反应的化学反应方程式为________________________ ;已知称取黄铁矿样品的质量为1.50g,称得灼烧后固体的质量为0.4g,不考虑操作误差
 ,则该矿石中FeS2的质量分数是________________。
,则该矿石中FeS2的质量分数是________________。 (10分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
| 实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | c | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=9 |
(
 2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________
2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是__________(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________________________________

(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mo
 l·L-1。
l·L-1。 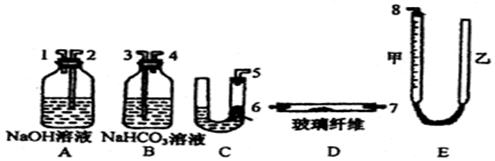
 表所列的实验目的,请选择合适的实验方法,将其标号填在答题上。
表所列的实验目的,请选择合适的实验方法,将其标号填在答题上。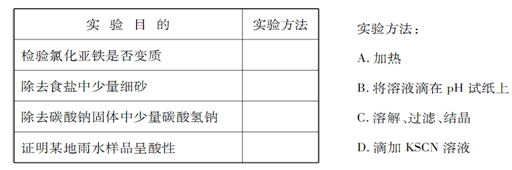

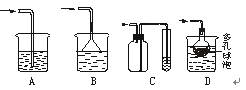
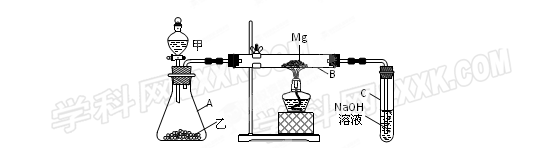 (1)选择制取SO2的最合适试剂 (填序号)。
(1)选择制取SO2的最合适试剂 (填序号)。
 ;
; 的实验并回答相关问题。
的实验并回答相关问题。 除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。
除尖嘴部分气泡后,使液面位于“0”刻度或“0”度以下。静置,读取数据并记录为NaOH标准溶液体积的初读数。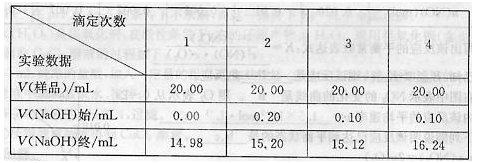
 NaOH溶液吸收过量的CO2气体,至CO2
NaOH溶液吸收过量的CO2气体,至CO2 气体不再溶解;
气体不再溶解;
 _,作用是_____________________________________________
_,作用是_____________________________________________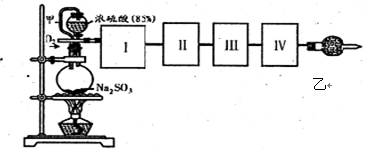
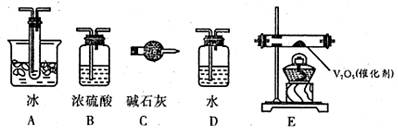
 催化剂与滴加浓硫酸的顺序中,应采取的操作
催化剂与滴加浓硫酸的顺序中,应采取的操作 变”或“降低”)。
变”或“降低”)。