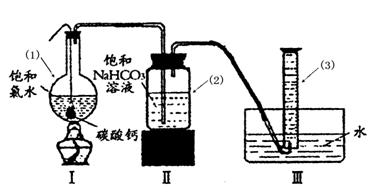
(10分)I.在足量的氯化亚铁溶液中加入少量(1—2滴)液溴,振荡后溶液变为黄色。
(1)甲同学认为是Br2单质溶于水变成黄色溶液;乙认为是Fe2+被氧化成Fe3+使溶液变成黄色。
(2)请根据提供试剂作出判断:
试剂: A 酸性高锰酸钾溶液 B 氢氧化钠溶液 C 四氯化碳 D 硫氰化钾溶液
判断: 两个同学的观点中正确的是__________(填 “甲” 或 “乙”), 并用两种方法(原理不同)加以试验证明, 写出选用的试剂编号及实验中观察到的现象:
| | 选用试剂 | 实验现象 |
| 第一种方法 | | |
| 第二种方法 | | |
Ⅱ.若要把溶解于水中的Br2单质分离出来,所需要的主要玻璃仪器是_____, 该操作的名称是_ _
(8分)用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.2000mol·L -1的氢氧化钠溶液(指示剂为酚酞)滴定得结果如下:
| | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.40mL | 18.50mL |
| 第二次 | 1.30mL | 18.05mL |
| 第三次 | 3.10mL | 21.20mL |
 色到 色;
色到 色;(2)根据以上数据可以计算出盐酸的物质的量浓度为 ;
(3)以下操作造成测定结果偏高的原因可能是 。
| A.滴定终点读数时,俯视滴定管的刻度,其它操作均正确 |
| B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
| C.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液 |
| D.未用标准液润洗碱式滴定管 |
浓硫酸与木炭粉在加热条件下反应:C+2H2SO4(浓) CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
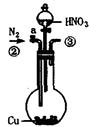
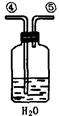
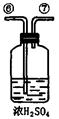
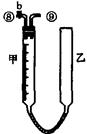
Ⅰ、第一小组用下图所示各装置设计一个实验,验证上述反应所产生的三种产物。 
(1)这些装置的连 接顺序(按产物气流从左到右的方向)是(填装置的编号):
接顺序(按产物气流从左到右的方向)是(填装置的编号): ④ →__________→__________→__________。
④ →__________→__________→__________。
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液变化体现了SO2 性,B瓶溶液反应是利用SO2 性。
B瓶溶液的作用是 ,
C瓶溶液的作用是 。
(3)实验时装置②中看到现象是 。
(4)装置③中所加的试剂名称是 ,现象是 。
Ⅱ、另一小组为测得CO2和SO2的质量,并算两者物质的量比,设计下列实验:
将生成气体依次通过X溶液→浓硫酸→碱石灰1→碱石灰2,并设法让气体完全被吸收。
(1)下列试剂中可以充当X的是: ( )
| A.BaCl2溶液 | B.Ba(OH)2溶液 |
| C.滴加H2O2的BaCl2溶液 | D.滴加H2O2的Ba(OH)2溶液 |
 增重质量为bg。用a、b表示CO2和SO2的物质的量比 。
增重质量为bg。用a、b表示CO2和SO2的物质的量比 。  主要成分是氯气,还含有少量空气和水蒸气。
主要成分是氯气,还含有少量空气和水蒸气。
 可与食盐制取浓HCl、浓HCl可与KMnO4制取C
可与食盐制取浓HCl、浓HCl可与KMnO4制取C l2,选用
l2,选用 下图所示装置(含有所盛放的试剂)设计实验。
下图所示装置(含有所盛放的试剂)设计实验。
 HCl,Cl2的化学反应方程式:
HCl,Cl2的化学反应方程式: _________________________________。
_________________________________。 0mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水使反应完全;
0mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水使反应完全;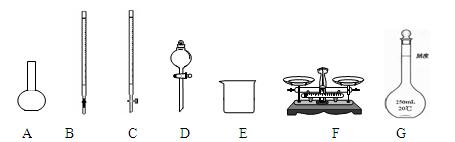

 入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若装置D中装的
入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若装置D中装的 是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。 酸 C.硝酸钾溶
酸 C.硝酸钾溶 液 D.硫化钠溶液
液 D.硫化钠溶液 l2与含X的溶液反应的离子方程式 。
l2与含X的溶液反应的离子方程式 。

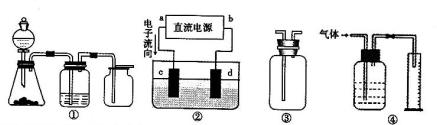
 ,a为正扳,d为阳极
,a为正扳,d为阳极 2、NH3、Cl2,、HCl、NO2等
2、NH3、Cl2,、HCl、NO2等 .装置④能用于测量气体体积
.装置④能用于测量气体体积

 向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是 ;
向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是 ;
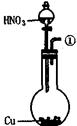
 氧化性,能把酸碱指示剂氧化褪色而影响实验。因此,中和滴定前必须进行的操作是 。
氧化性,能把酸碱指示剂氧化褪色而影响实验。因此,中和滴定前必须进行的操作是 。 越大。
越大。
 + H+ Ka1(H2CO3)=4.45×10—7
+ H+ Ka1(H2CO3)=4.45×10—7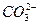 +H+ Ka2(HCO3-)=5.61×10-11
+H+ Ka2(HCO3-)=5.61×10-11 Ka(HClO)=2.95×10-8
Ka(HClO)=2.95×10-8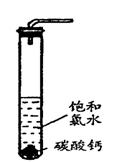
 面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。