(10分)某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算合金样品中镁的质量分数。
(3)计算所用稀硫酸中H2SO4的质量分数。
为了测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
| A.冷却至室温后,在250mL容量瓶中定容配成250mL稀硫酸。 |
| B.用某仪器量取25.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
| C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为M mol/L的标准NaOH溶液装入碱式滴定管,调节液面记下开始读数为V1mL。 |
F、把锥形瓶移到碱式滴定管下,在锥形瓶下垫一张白纸。
G、用某仪器准确量取浓硫酸样品10.00 mL,在烧杯中用蒸馏水溶解。
就此实验操作完成下列填空:
⑴正确操作步骤的顺序(用编号字母填写) → A → → →→ → 。
⑵用来量取10.00mL浓硫酸的仪器是 。用NaOH溶液润洗碱式滴定管的目的是 。
⑶滴定中可选用的指示剂是 。滴定中,目光应注视_____ ;判断滴定恰好完成的依据是____;读数时,目光与凹液面的最低处保持水平。
⑷某学生实验时用稀硫酸润洗了锥形瓶测定的浓度会偏_。(填“偏高”、“偏低”、“无影响”)
⑸该浓硫酸样品的浓度计算式为 ___________ 。
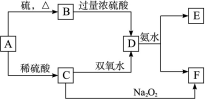

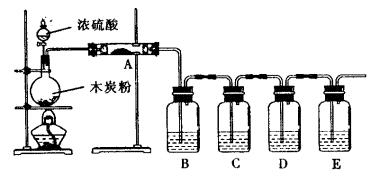
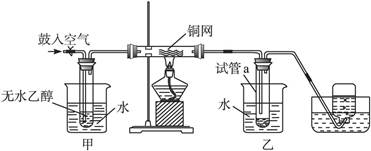
 某研究性小组借助A-D的仪器装置完成有关实验
某研究性小组借助A-D的仪器装置完成有关实验
 和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。
和镀层厚度,查询得知锌易溶于碱:Zn+2NaOH=Na2ZnO3+H2↑据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1 g。用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验。 = 。
= 。