(8分)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。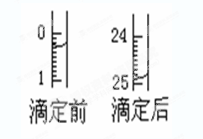
(1)滴定
①用______式滴定管盛装0.1000 mol/L盐酸标准 液,锥形瓶中装有25.00mL待测烧碱溶液。上图表示某次滴定时50 mL滴定管中前后液面的位置。请将用去的标准盐酸的体积填入②表空格中。
②有关数据记录如下:
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 25.00 | 0.50 | 25.95 | 25.45 |
| 2 | 25.00 | 0.30、 | | |
| 3 | 25.00 | 6.00 | 31.55 | 25.55 |
c(NaOH) = _____________ 。
(3)读数时,若滴定前仰视,滴定后俯视,则会使最终测定结果_________。(填“无影响”、“偏高”、“偏低”)
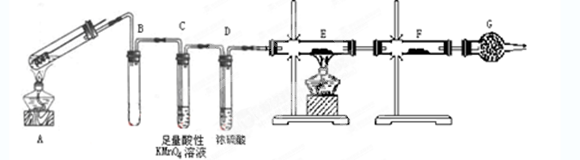
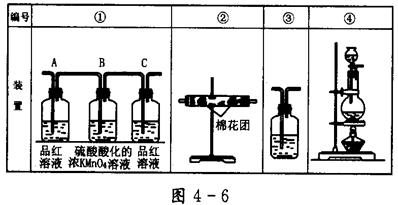
(12分)〔Ⅰ〕某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下实验流程图:
请回答以下问题:
(1)为验证气体A,按右图所示装置进行实验:若能观察到酸性高锰酸钾溶液褪色,即可证明火柴头上含有S元素,请写出气体A使酸性高锰酸钾溶液褪色的离子方程式 。
(2)步骤②的实验操作装置如右图所示,该操作的名称是 ,其优点是 ;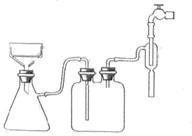
(3)指出图中的错误:
错误① 。
错误② 。
错误③ 。
(有几个错误写几个,不一定要填满)
〔Ⅱ〕以下是牙膏中某些主要成分的检验的实验流程图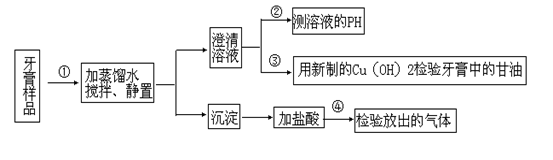
(1)关于上述实验说法不正确的是:
| A.在①中,可用倾析法分离溶液和沉淀; |
| B.在②中,测得PH﹥7,可能是牙膏成分中NaF水解引起的; |
| C.在③中,用新制Cu(OH)2检验会出现绛蓝色沉淀; |
| D.在④中,放出的气体通过澄清石灰水不一定出现沉淀; |
(12分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下两种方法:
I.还原法 在酸性介质中用FeSO4等将+6价铬还原成+3价铬。具体流程如下:
有关离子完全沉淀的pH如下表:
| 有关离子 | Fe2+ | Fe3+ | Cr3+ |
| 完全沉淀为对应氢氧化物的pH | 9.0 | 3.2 | 5.6 |
(2)还原+6价铬还可选用以下的________________试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
则在操作②中可用于调节溶液pH的试剂为:_____________(填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
此时调节溶液的pH范围在____________(填序号)最佳。
A.3~4 B.6~8 C.10~11 D.12~14
II.电解法 将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72一发生反应,生成的Fe3+和Cr3+在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(4)写出阴极的电极反应式______________________________________。
(5)电解法中加入氯化钠的作用是:_______________________________________。