(14分)右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题
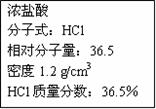  |
(2)配制250mL 0.1mol/L的盐酸溶液
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
| | |
B.将已冷却的盐酸沿玻璃棒注入容量瓶中。
C.用蒸馏水洗涤 2—3次,洗涤液均注入容量瓶,振荡。
D.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm
 处,改用 加水,使溶液凹面恰好与刻度相切。
处,改用 加水,使溶液凹面恰好与刻度相切。E.将容量瓶盖紧,振荡,摇
 匀。
匀。(3) 若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水 ;
②向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,则浓度 ;
③定容时俯视容量瓶刻度线 。
(4)实验室里迅速制备少量氯气可利用以下反应:2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O 此反应不需要加热,常温下就可以迅速进行。
①用“双线桥法” 标明电
 子转移的方向和数目:
子转移的方向和数目:2 KMnO4+16 HCl ="==" 2 KCl + 2 MnCl2 + 5 Cl2↑ + 8 H2O
②用该浓盐酸制得了标况下560mlCl2,则被氧化的HCl为 mol,需要KMnO4的质量 g
(12分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
【实验设计】控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表)。设计如下对比实验。
(1)请完成以下 实验设计表(请填满表中空缺地方,表中不要留空格)。
实验设计表(请填满表中空缺地方,表中不要留空格)。
| 实验编号 | 实验目的 | T/K | pH |  c/10-3mol·L-1 c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验做参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | | | | |
| ③ | | 298 | 10 | 6.0 | 0.30 |
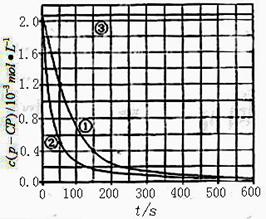
【数据处理】实验测得p-CP的浓度随时间变化的关系如右上图。
(2)请根据右上图实验①曲线,计算降解反应在50 -150
 内的反应速率ν(p-CP )=
内的反应速率ν(p-CP )= 【解释与结论】
(3)实验①②表明温度升高,降解反应速率增大。但
 温度过高时反而导致降解反应速率减小,请从Fenton法所使用试剂H2O2的角度分析原因: ;
温度过高时反而导致降解反应速率减小,请从Fenton法所使用试剂H2O2的角度分析原因: ;(4)实验③得出的结论是:pH=10时, ;
【思考与交流】
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来,根据上图中信息,给出一种迅速停止反应的方法:
 。
。 (6分)除去下列物质中的杂质(括号中的物质为杂质),请填表中空白处:
| 物质 | 加入试剂 | 离子方程式 |
| KCl(K2CO3) | .Com] | |
| FeCl3(FeCl2)溶液科 | [网] | |
| FeSO4 (CuSO4) 溶液 | | |
 ①称量NaCl时,物码倒置(
①称量NaCl时,物码倒置( 1 g以下用游码)________________________________
1 g以下用游码)________________________________  __________________________________________________
__________________________________________________ ______________________。
______________________。 1)用移液管量取20.00 mL FeSO4溶液放入锥形瓶中,用0.10 mol·L-1的酸性KMnO4溶液滴至终点,耗去KMnO4溶液20.00 mL,若生成物中Mn元素全部呈+2价,滴定反应的离子方程式为______ __,据此可测得FeSO4溶液的物质的量浓度为______ __mol·L-1。
1)用移液管量取20.00 mL FeSO4溶液放入锥形瓶中,用0.10 mol·L-1的酸性KMnO4溶液滴至终点,耗去KMnO4溶液20.00 mL,若生成物中Mn元素全部呈+2价,滴定反应的离子方程式为______ __,据此可测得FeSO4溶液的物质的量浓度为______ __mol·L-1。 有A13+、Cu2+。。K+、NH4+ .C1-——等离子,现通过如下实验对其中的阳离子进行检验:——
有A13+、Cu2+。。K+、NH4+ .C1-——等离子,现通过如下实验对其中的阳离子进行检验:—— 溶液,实验操作步骤有:
溶液,实验操作步骤有: 的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)
的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)
 ,相应的离子方程式为 。
,相应的离子方程式为 。