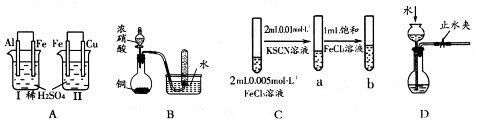
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
| A.取a克混合物充分加热,减重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
下列实验不能达到预期目的的是
| 代号 | 实 验 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯与溴的非金属性强弱 |
| B | 同温下测定相同浓度的Na2CO3, 和Na2SO4溶液的酸碱性 | 比较硫酸与碳酸的酸性强弱 |
| C | AlCl3、MgCl2溶液中通人过量氨气 | 比较镁与铝单质的还原性强弱 |
| D | 同温下用同一电路分别测定同浓度的 盐酸和某一元酸溶液导电能力 | 比较该一元酸与盐酸酸性的强弱 |
某同学如图所示装置进行实验,当滴入液体后出现气球体积缩小了,则使用的固体和液体试剂可能是( )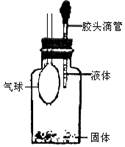
| A.铜与浓硫酸 | B.铁与浓硫酸 |
| C.铝和氢氧化钠溶液 | D.二氧化锰和浓盐酸 |
下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe 粉中加入稀HNO3,充分反应后,滴入KSCN 溶液 | 溶液呈红色 | 稀HNO3将Fe 氧化为Fe3+ |
| B | 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水 | 有白色沉淀出现 | 该钾盐是K2CO3 |
| C | Al 箔插入稀HNO3中 | 无现象 | Al 箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
孔雀石的主要成分为xCuCO3·yCu(OH)2·zH2O,为测定其中CuCO3的质量分数,称取a g样品进行实验。下列实验方案可行的是
| A.充分加热样品,用碱石灰吸收逸出气体,增重b g |
| B.加热至样品质量不再发生变化,称得其质量为b g |
| C.向样品中加入足量的稀盐酸,用排水法收集逸出气体,得b mL气体 |
| D.向样品中加入足量的稀盐酸,充分反应,将生成的气体全部通入到足量Ba(OH)2溶液中,过滤、洗涤、烘干,得b g固体 |
下列家庭化学小实验不能达到预期目的的是
| A.用米汤检验食用加碘盐(含KIO3)中含有碘元素 |
| B.用醋、石灰水验证蛋壳中含有碳酸盐 |
| C.用碘酒检验汽油中是否含有不饱和烃 |
| D.用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
用一充满氨气的烧瓶做喷泉实验,当水充满整个烧瓶后,烧瓶内的氨水的物质的量浓度是(按标准状况下计算)
| A.1mol·L-1 | B.0.045mol·L-1 | C.0.029mol·L-1 | D.不能确定 |
下列实验过程中,始终无明显现象的是 ( )
| A.NO2通入FeSO4溶液中 |
| B.CO2通入CaCl2溶液中 |
| C.NH3通入AlCl3溶液中 |
| D.SO2通入已酸化的Ba(NO3)2溶液中 |
下列化学实验事实及其解释都正确的是
| A.因为Ksp(CaCO3)<Ksp(CaSO4),所以可用Na2CO3和HCl除去水垢中的CaSO4 |
| B.粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强 |
| C.滴有酚酞的碳酸氢钠溶液呈浅红色,微热后红色加深,是因为碳酸氢钠分解生成了碳酸钠 |
D.硫化钠溶于水中发生反应的离子方程式为S2 –+ 2H2O H2S + 2OH – H2S + 2OH – |