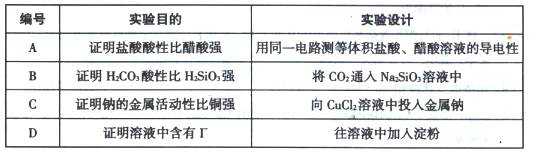
实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是
| A.酸式滴定管在装液前未用标准酸溶液润洗2~3次 |
| B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 |
| C.滴定前平视读数,滴定后俯视读数 |
| D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次 |
下列装置或操作能达到实验目的的是 ( )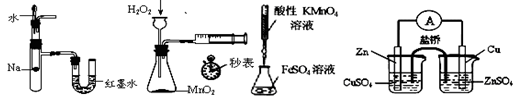
| A.验证反应的热效应 | B.定量测定化学反应速率 |
| C.滴定法测FeSO4 | D.构成铜锌原电池溶液的浓度 |
喷泉是一种常见的自然现象。图1为化学教材中的喷泉实验装置。该生积极思考,只要满足烧瓶内压强与玻璃管水柱压强的和小于烧瓶外的压强就可以产生喷泉。于是他设计了图2所示的装置。在图2的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )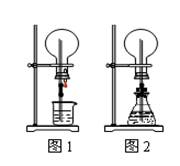
| A.Cu和稀盐酸 | B.NaHCO3与NaOH溶液 |
| C.MnO2与稀盐酸 | D.Na2CO3与稀盐酸 |
下列实验“操作和现象”与“结论”都正确的是
| | 操作和现象 | 结论 |
| A | 切开金属钠,钠表面的银白色会逐渐褪去 | Na在空气中会生成Na2O2 |
| B | 铝箔插入浓硝酸中,无明显现象 | 铝与浓硝酸不反应 |
| C | SO2通入酸性KMnO4溶液,溶液褪色 | SO2具有漂白性 |
| D | 将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的2/3处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 | 从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
某同学对下列四个实验都设计了两种方案,其中两种方案均合理的是
| 选项 | A | B | C | D |
| 实验 目的 | 除去碳酸钠中少量的碳酸氢钠 | 清洗铁制品 表面的铁锈 | 检验苯中 含有少量甲苯 | 鉴别二氧化氮 和溴蒸汽 |
| 方案1 | 溶解后加入盐酸 | 加适量稀盐酸 | 加入Br2/CCl4 | 加水 |
| 方案2 | 加热 | 用水洗涤 | 加入酸性KMnO4 | 加压 |
有①②③三瓶体积相等,浓度都是1mol/L的HCl溶液,将①加热蒸发至体积减小一半,在②中加少量CH3COONa固体(加入后溶液仍呈酸性),③不作改变,然后以酚酞作指示剂,用NaOH溶液滴定上述三种溶液,所消耗的NaOH溶液的体积是
| A.①<②=③ | B.③>②>① | C.①=②=③ | D.①=③>② |
下列实验能够达到预期目的的是:
| A.在一支盛有2mL 2% CuSO4溶液的试管中,滴入几滴10%的NaOH溶液,再加入1mL乙醛溶液,加热后可以看到红色氧化亚铜沉淀生成 |
| B.将乙酸乙酯与NaOH溶液混合并用水浴加热,即可得到水解产物乙醇和乙酸 |
| C.检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入NaOH溶液中和硫酸,再加入银氨溶液加热 |
| D.在一支试管中滴入10滴溴乙烷,再加入1mL 5%的NaOH溶液,共热后滴加硝酸银溶液,可观察到有浅黄色溴化银沉淀生成 |
下列实验操作正确的( )
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.提取碘水中的碘单质时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| C.用PH试纸测定某无色溶液的PH时,应将PH试纸放入溶液中,观察其颜色变化,跟标准比色卡比较 |
| D.蒸馏操作中,温度计应该放在蒸馏烧瓶内的液体中,以测量液体的温度 |