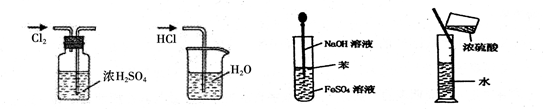
下列实验方案设计中,可行的是( )
| A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 |
| B.用萃取的方法分离汽油和煤油 |
| C.用溶解过滤的方法分离KNO3和NaCl固体的混合物 |
| D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 |
下列有关实验原理或操作正确的是
| A.仅用硝酸银溶液便可鉴别亚硝酸钠和食盐 |
| B.减压过滤是为了加快过滤速度,得到较大颗粒的晶体 |
| C.硫酸亚铁铵晶体过滤后用无水乙醇洗涤 |
| D.纸层析法分离铁离子和铜离子实验中,展开剂的成份为蒸馏水与丙酮 |
海洋中有丰富的食品、矿产,能源、药物和水产资源等(如下图所示)下列有关说法正确的是( )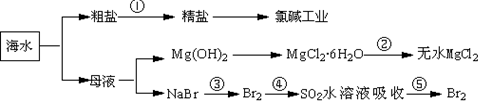
| A.第①步中除去粗盐中的S042-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2C03溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
| B.第②步中结晶出的MgCl2?6H20可在空气中受热分解制无水MgCl2 |
| C.在第③④⑤步中溴元素均被氧化 |
| D.大量的氮、磷废水排入海洋,易引发赤潮 |
不能鉴别AgNO3、BaCl2、K2CO3和Mg(NO3)2四种溶液(不考虑他们之间的相互反应)的试剂组是 ( )
| A.盐酸、硫酸 | B.盐酸、氢氧化钠溶液 |
| C.氢氧化钠溶液、硫酸 | D.氨水、氢氧化钠溶液 |
(8分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液,选择甲基橙作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_____________,滴定终点的判断方法是________________________。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是 .
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
下列实验方案的设计或实验过程的评价中,正确无误的是( )
| A.某溶液中加入BaCl2溶液产生白色沉淀,说明一定含SO42- |
| B.除去生石灰中的石灰石,可加水后进行过滤 |
C.某无色溶液中滴入紫色石蕊 试液显红色,说明该溶液呈碱性 试液显红色,说明该溶液呈碱性 |
| D.可以用溶解、过滤、蒸发的方法除去BaCl2中的BaSO4 |
下列实验不能达到预期目的是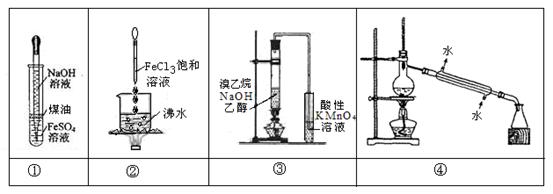
| A.实验①:挤出胶头滴管中的NaOH溶液,观察Fe(OH)2沉淀的颜色 |
| B.实验②:继续煮沸溶液至红褐色,停止加热,当光束通过体系时产生丁达尔效应 |
| C.实验③:通过观察酸性KMnO4溶液紫色褪去,确认有乙烯生成 |
| D.实验④:控制一定温度,将石油分离为汽油、柴油等 |
下列实验装置能达到实验目的是(夹持仪器未画出)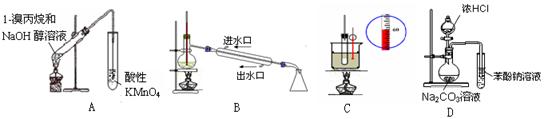
| A.A装置用于检验溴丙烷消去产物 | B.B装置用于石油的分馏 |
| C.C装置用于实验室制硝基苯 | D.D装置可装置证明酸性:盐酸>碳酸>苯酚 |
有一无色溶液,可能大量含有K+、A13+、Ba2+、NH4+、Cl-、SO42-、SO32-、HCO3-中的几种。为确定其成分,做如下实验:①取部分溶液,加入足量Na2O2固体,有气体产生,最后也有沉淀产生;②另取①中静置后少量上层清液,加入足量硝酸酸化的AgNO3溶液,但最后没有白色沉淀产生。下列推断正确的是
| A.可能有A13+、NH4+、Cl- | B.肯定有A13+、Ba2+、HCO3- |
| C.可能没有K+、HCO3-、NH4+ | D.肯定没有A13+、SO32-、SO42- |