要配制浓度约为2 mol/L NaOH溶液100 mL,下面的操作正确的是 ( )
| A.用托盘天平称取8 g NaOH固体(NaOH固体放置于天平的托盘上),放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B.称取8 g NaOH固体,放入100 mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL |
| C.称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| D.用100 mL量筒量取40 mL 5 mol/L NaOH溶液,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,在不断搅拌下慢慢倒入烧杯中 |
人造光卤石(KCl·MgCl2·6H20)是盐化工生产的中间产物。以光卤石为原料制得金属镁,可有下列步骤:
①过滤②溶解 ③加入适量Ca(OH)2④蒸发⑤用盐酸溶解⑥电解熔融MgCl2 ⑦在HCl气流中强热MgCl2·6H20晶体正确的顺序是
| A.⑤③①②④⑥⑦ | B.②③①⑤④⑦⑥ |
| C.②④①③⑦⑤⑥ | D.⑤③①④②⑦⑥ |
下列实验方案可行的是
| A.检验氯乙烷中的氯元素时,将氯乙烷和NaOH溶液混合加热后,用稀硫酸进行酸化 |
| B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液进行酸化 |
| C.除去苯中的甲苯,依次加高锰酸钾溶液、NaOH溶液,然后用分液漏斗分液 |
| D.检验CH3—CH==CH—CHO分子中醛基,可用溴水或银氨溶液。 |
某学生做乙醛还原性的实验,取2 mL 1 mol·L-1的硫酸铜溶液和4 mL 0.4 mol·L-1的氢氧化钠溶液,在一个试管内混合后,加入0.5 mL 40%乙醛溶液加热至沸,无砖红色沉淀。实验失败的原因是
| A.氢氧化钠不够量 | B.硫酸铜不够量 |
| C.乙醛溶液太少 | D.加热时间不够 |
可以把6种无色溶液:乙醇、苯酚、甲苯、AgNO3溶液、KOH溶液、硫化氢一一区分的试剂是( )
| A.新制碱性Cu(OH)2悬浊液 | B.FeCl3溶液 |
| C.BaCl2溶液 | D.酸性KMnO4溶液 |
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: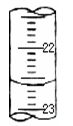
①用0.1000mol/L的标准盐酸润洗酸式滴定管2~3次
②取标准盐酸注入酸式滴定管至“0”刻度以上2~3mL处
③把盛有标准盐酸的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液
④调节液面至“0”或“0”刻度以下,记下读数
⑤取20.00mL待测NaOH溶液注入洁净的锥形瓶中,并加入2~3滴甲基橙试液
⑥把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点,记录滴定管读数
请回答下列问题:
(1)判断到达滴定终点的现象是 。
(2)某次滴定时的滴定管中的液面如右图所示,其读数为 mL。
(3)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
(4)下列实验操作会使实验结果偏高的是 。
A、锥形瓶用待测液润洗后再注入待测液
B、酸式滴定管未用标准液润洗,便装入标准液
C、酸式滴定管滴定前俯视读数,滴定后仰视读数
D、酸式滴定管滴定前有气泡,滴定后无气泡
下列能达到实验目的的是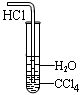
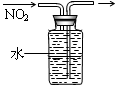
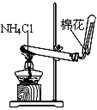
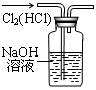
| A.防倒吸 | B.排水法收集NO2 | C.实验室制氨气 | D.除去杂质气体HCl |
下列实验方法使用不合理的是
| A.用结晶法从水溶液中获得氯化铁晶体 |
| B.用纸上层析法检验氯化铁溶液中是否混有少量氯化铜 |
| C.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量必需相等 |
| D.用AgNO3溶液、稀硝酸鉴别亚硝酸钠和食盐 |
