某研究小组设计了如图所示的循环系统,来生产能解决能源危机的某种物质,其中所需的电能由太阳能光电池提供。有关叙述正确的是 ( )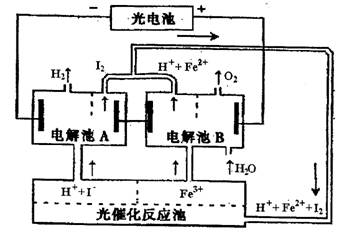
|
| A.设计该循环系统的目的是制取I2 | B.电解池A中离子反应方程式: |
C.光催化反应池中离子反应方程式为: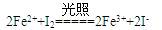 | |
| D.该系统中的Fe3+、H2O、I-都是循环使用的物质 |
下列有关滴定操作顺序正确的是 ( )
①检查滴定管是否漏水 ②用蒸馏水洗涤玻璃仪器 ③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管 ④装标准溶液和待测液并调整液面(记录初读数) ⑤取一定体积的待测液于锥形瓶中 ⑥滴定操作
| A.①③②④⑤⑥ | B.①②③④⑤⑥ |
| C.②③①④⑤⑥ | D.④⑤①②③⑥ |
某同学设计如下实验测量m g铜银合金样品中铜的质量分数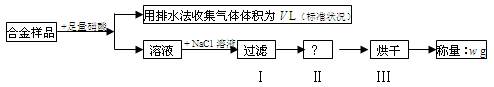
下列说法中不正确的是
| A.收集到的V L气体全为 NO |
| B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒 |
| C.操作Ⅱ应是洗涤 |
D.铜的质量分数为: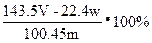 |
实验室常用如图所示的两套装置测量所制得的气体体积,下面有关此两套量气装置的使用说明不正确的是 ( )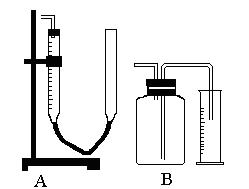
| A.用B量气前,广口瓶中通常应盛满相应的液体 |
| B.用A量气前,测量管中应充满相应的液体 |
| C.收集完气体后,在读数前应使盛液管内(量筒)液面与集气管(瓶)体的容器内液面相平 |
| D.A是直接测量气体体积而B直接测量的是液体的体积 |
下述实验不能达到预期实验目的的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 将2.5g CuSO4·5H2O溶解在97.5g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
| B | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
下列有关实验操作的说法正确的是( )
| A.SO2通入酸性高锰酸钾溶液中,溶液褪色,说明SO2具有漂白性 |
| B.用蒸馏水将PH试纸先润湿,可用于检验氨气 |
| C.可用瓷坩埚熔化各种钠的化合物 |
| D.某溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
由实验事实得出的结论,其中正确的是
| | 实验事实 | 结论 |
| A | NH3的水溶液能导电 | NH3是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | Ca(ClO)2溶液中通入CO2产生白色沉淀 | 酸性:H2CO3 >HClO |
| D | Na2SiO3溶液中滴入盐酸,产生白色沉淀 | 非金属性:Cl>Si |
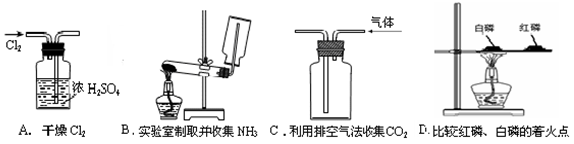
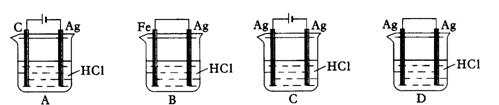
 2AgCl + H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是
2AgCl + H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是