(13分)Ⅰ下列实验操作、现象、结论、说法不正确的是_______________(填序号)
①.苯酚沾在手上立即用酒精洗涤
②.除去淀粉中的少量氯化钠,可以加蒸馏水,用渗析的方法
③.向蛋白质溶液中加入CuSO4盐溶液会使蛋白质发生盐析
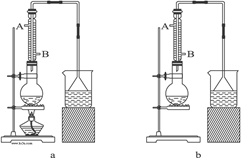
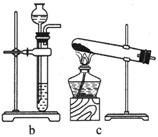
④.制取乙酸乙酯用如右图所示的实验装置
⑤.区别植物油和直馏汽油的正确方法是将它们分别滴入溴水当中,稍加振荡,
观察溴水的颜色是否褪去
⑥.在溴乙烷中加入NaOH水溶液并加热,水层中加入足量HNO3酸化,再滴入AgNO3溶液以检验其是否发生水解
⑦.皂化反应完成后加入食盐可以使高级脂肪酸钠从混合物中析出,这一过程叫盐析
⑧.在蔗糖溶液中滴加几滴稀硫酸,微热,加入新制Cu(OH)2悬浊液煮沸,通过观察有无砖红色沉淀生成来检验蔗糖水解产物是否含有葡萄糖
Ⅱ 实验室需要0.5 mol/L硫酸溶液480mL。回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_____________(填序号),配制上述溶液还需用到的玻璃仪器是________________(填仪器名称)。
(2)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为__________mL(计算结果保留一位小数)。
(3)配制时,该同学的操作顺序如下,请将操作步骤C补充完整。
| A.用量筒准确量取所需的浓硫酸,沿玻璃棒倒入盛有适量水的烧杯中。并用玻璃棒不断搅拌至冷却 |
| B.将烧杯中的硫酸沿玻璃棒注入所选的容量瓶中① |
| C._______________________________________________________________________ |
| D.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm 处 |
F.将容量瓶盖紧,振荡,摇匀
(4)若实验遇到下列情况,会导致硫酸溶液的物质的量浓度偏低的是__________(填序号)
①用以稀释硫酸的烧杯未洗涤
②量取浓硫酸的量筒未洗涤
③摇匀后发现液面低于刻度线再加水
④容量瓶中原有少量蒸馏水
⑤定容时观察液面俯视
(15分)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、冰醋酸,D中放有饱和碳酸钠溶液。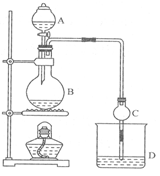
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用:________________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:___________________ _____。
(2)球形干燥管C的作用是____________________________。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示)______________________ _;反应结束后D中的现象是_________________________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;然后再进行 (此空从下列选项中选择)_________操作,以得到较纯净的乙酸乙酯:
A.淬取 B.蒸发 C.蒸馏 D.分液
(16分)
(I)氧化还原反应Cu+2AgNO3=Cu(NO3)2+2Ag可设计成一个原电池,
写出两个电极上的电极反应:负极:____________,正极:_____________。
(II)已知NaHCO3水溶液呈碱性:
(1)用离子方程式表示NaHCO3溶液呈碱性的原因__________________
(2) NaHCO3溶液中各离子的浓度由大到小的关系是________________
(III)某温度下,密闭容器中A、B、C三种气体的初始浓度和平衡浓度如下表:
| 物质 | A | B | C |
| 初始浓度/mol?L—1 | 0.020 | 0.020 | 0 |
| 平衡浓度/mol?L—1 | 0.016 | 0.016 | 0.0080 |
(1)反应达到平衡时,A的转化率为_____________。
(2)该反应的化学方程式可表示为(用A、B、C表示物质的化学式)
_____________________________,其平衡常数为_______________。
(3)该温度下,若将A和B各0.10mol的气体混合物充入10L的密闭容器中发生反应,10s末达到平衡,则用A表示的化学反应速率为____________________。
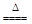 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O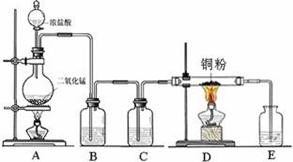
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
 2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。
2Fe2++I2,有资料认为这可能是一个可逆反应。Fe3+与I-反应后的溶液显深红色,它是I2溶于KI溶液的颜色。为探究该深红色溶液中是否含Fe3+,进而证明这是否是一个可逆反应,试利用实验室常用仪器、用品及以下试剂设计方案并填写位于答题卷的下表。0.1 mol/L的FeCl3、KI、KSCN、NaOH、H2SO4、KMnO4溶液,CCl4,蒸馏水。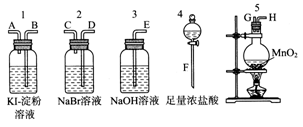




 生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。
生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。 ,然后进行的实验操作是 (填写正确选项的字母)。
,然后进行的实验操作是 (填写正确选项的字母)。 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液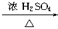 C2H5Br+H2O
C2H5Br+H2O