(8分)
氯化铵是一种重要的化工原料,应用广泛。
(1)实验室通常用NH4Cl固体与Ca(OH)2固体混合共热制取氨气。
写出实验室制取氨气的反应方程式 。
(2)用浓氯化铵溶液处理的舞台幕布难着火,其原因是 (填字母)。
①幕布的着火点升高 ②幕布的质量增加 ③氯化铵分解吸收热量,降低了温度
④氯化铵分解产生的气体隔离了部分空气
| A.①② | B.③④ | C.①③ | D.②④ |
NaNO2+NH4Cl
 NaCl+N2↑+2H2O实验装置如图所示,试回答:
NaCl+N2↑+2H2O实验装置如图所示,试回答: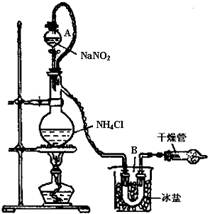
①装置中A部分的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是 (填写编号)。
a.防止饱和溶液蒸发
b.保证实验装置不漏气
c.使饱和NaNO2溶液容易滴下
②加热前必须进行的一个操作步骤是 。
使用酸碱中和滴定法测定市售白醋的总酸量(g/100 mL)。
Ⅰ.实验步骤:
(1)配制100 mL待测白醋溶液。量取10.00 mL市售白醋,注入烧杯中用水稀释后转移到 (填仪器名称)中定容,摇匀即得。
(2)用 量取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2_____作指示剂。
(3)读取盛装0.100 0 mol·L-1 NaOH溶液的 (填仪器名称)的初始读数。如果液面位置下图所示,则此时的读数为 mL。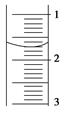
(4)滴定。滴定过程中,眼睛应观察 。滴定终点后记录NaOH溶液的终点读数。再重复滴定3次。
Ⅱ.实验记录:
| 滴定次数 实验数据/mL | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(1)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积V=[(15.95+15.00+15.05+14.95)/4] mL=15.24mL。
指出他的计算的不合理之处:______________________________________。
按正确数据处理,可得c(市售白醋)=___________mol·L-1;市售白醋总酸量=_________g/100 mL。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是_______ (填写序号)。
a.未用标准NaOH溶液润洗滴定管
b.锥形瓶中加入待测白醋溶液后,再加少量水
c.锥形瓶在滴定时剧烈摇动,有少量液体溅出
d.滴定前锥形瓶用待测白醋溶液润洗
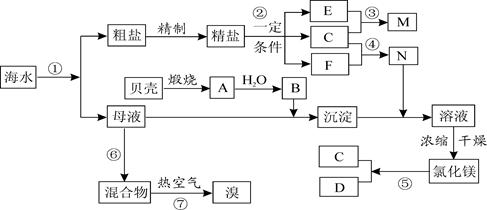
 单质处循环
单质处循环 (填“甲”或“乙”),理由是 。
(填“甲”或“乙”),理由是 。
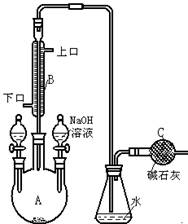
 +Br+→[
+Br+→[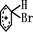 ];[
];[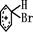 ]+FeBr4-→
]+FeBr4-→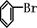 +HBr+FeBr3;
+HBr+FeBr3; +Br2→
+Br2→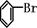 +HBr中的催化剂为( )
+HBr中的催化剂为( )