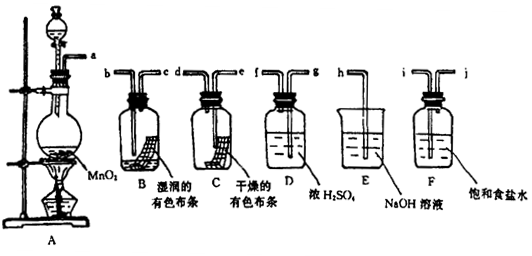
(15分) Ⅰ、某同学用下图所示装置(尾气吸收装置未画出)向溶液Y中通入NH3和CO2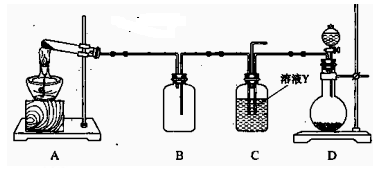
(1)下列为实验室制备NH3和CO2的备选药品:
a.NH4Cl b.CaCO3(块状) c.Ca(OH)2 d.NaOH e.浓氨水
f.稀盐酸 g.稀硫酸
则上述装置A处的试管中所放药品的最佳选择为 (用药品序号填
空,下同);装置D处固体药品的最佳选择为 (用药品序号填空)。
(2)下列各项制备实验中,也可利用装置D处仪器完成的是 (填序号)。
| A.MnO2与浓盐酸反应制备Cl2 | B.Cu与浓硫酸反应生成SO2 |
| C.由H2O2分解制O2 | D.乙醇与乙酸反应制备乙酸乙酯 |
(3)写出上述装置A处的试管中所发生反应的化学方程式:
。
Ⅱ、甲同学利用下图所示装置探究SO2和Cl2两种气体按不同比例混合后的漂白性。
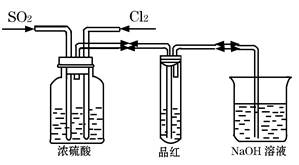
试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是:
。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: (结合反应方程式)。
实验题(10分)
⑴实验室配制500 mL 0.1mol/L的氢氧化钠,请回答下列问题:
①称量氢氧化钠固体时应放在 中进行:
②配制溶液时应选用 容量瓶;
③ 在此配制过程中胶头滴管的作用是 ;
在此配制过程中胶头滴管的作用是 ;
④若实验时遇到下列情况,将会使所配的溶液浓度发生什么变化:
容量瓶内壁沾有水滴没有烘干就进行配制 。(填“偏高”“偏低”或“无影响”):
⑵(在实验室中进行以下实验,请填写实验报告
| 实验步骤 | 现象及离子方程式 |
| ①向盛有2mL Na2SO4溶液的试管里加入2mL BaCl2溶液 | |
| ②向盛有2mL NaOH稀溶液的试管里滴入几滴酚酞溶液,再用滴管向试管里慢慢滴入稀盐酸,至溶液恰好变色为止 | |
(15分)氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液.制备出之后要冷却为固态才便于操作和贮存。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,铁架台和夹持仪器已略去。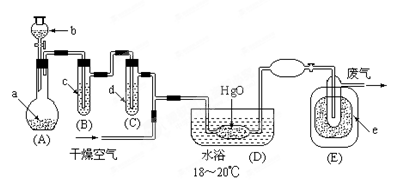
部分物质的有关物理数据如下:?
| 化学式 | 熔点(单位:℃) | 沸点(单位:℃) |
| N2 | -209.86 | -195.8 |
| O2 | -218.4 | -183 |
| CO2 | -57 | / |
| NH3 | -77.3 | -33.35 |
| Cl2 | -101 | -34.6 |
(1)A中盛有深色固体试剂a是 ,分液漏斗中b试剂是 。
(2)B中盛有液体c是 ,C中的液体d是 。?
(3)D中发生化学反应的化学方程式是 。
(4)E中的保温瓶中盛有致冷剂,它应是 (在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是 。
(5)装置A、B、C间的连接方式与D、E间的连接方式有明显的区别,这区别是 ,用这些不同的连接方式的主要理由是 。
 8分,每空2分)
8分,每空2分)

 不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是 。
不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是 。