(14分)某校化学课外活动小组利用下面所提供的仪器装置和药品制取NaHCO3溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2%NaOH溶液 ②稀HCl ③稀H2SO4 ④饱和KHCO3溶液 ⑤浓H2SO4 ⑥CaCO3固体 ⑦K2CO3粉末
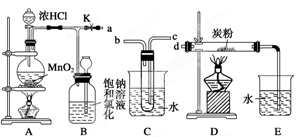
仪器装置(如图所示):
请根据题目要求回答下列问题: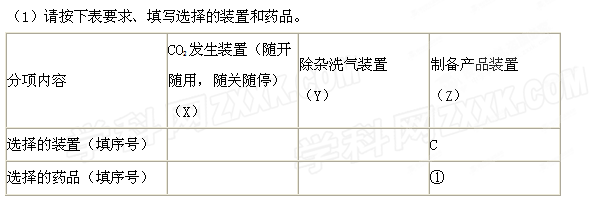
(2)如何检验所选择的CO2发生装置(X)的气密性,请写出主要操作过程: 。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为 ,Y装置中除去的杂质为 。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其原因是 ;通入 过量CO2后,Z装置内的溶液中离子浓度大小顺序为 ;若要保证乙装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过 %(质量分数)。
过量CO2后,Z装置内的溶液中离子浓度大小顺序为 ;若要保证乙装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过 %(质量分数)。
附:有关物质在常温(20℃)时的溶解度
| 化学式 | Na2CO3 | NaHCO3 | NaOH | NaCl | Na2SO4 |
| 溶解度(g/100gH2O) | 21.3 | 9.60 | 107 | 35.8 | 19.4 |
(4分)下列有关实验的叙述,正确的是(填序号)
| A.用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶 |
| B.用渗析法分离淀粉中混有的NaNO3杂质 |
| C.无法用分液漏斗将乙二醇和水的混合液体分离 |
| D.用浓氨水洗涤做过银镜反应的试管 |
拌
F.用酸式滴定管量取20.00mL 0.1000mol/L的KMnO4溶液
G.用托盘天平称取10.50g干燥的NaCl固体
H.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次
I.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物
J.配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀
刚好溶解为止

 行相关性质实验。(实验装置如右图所示)
行相关性质实验。(实验装置如右图所示)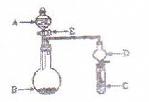


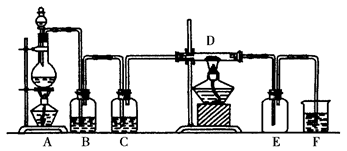

 2SO4的体积为 。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是 。(填序号)
2SO4的体积为 。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是 。(填序号)
 ),检验溶液A中Fe3+的最佳试剂为 (填代号)。
),检验溶液A中Fe3+的最佳试剂为 (填代号)。
 )欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时俯视容量瓶的刻度线,会使配制的浓度 。(填“偏高”、“偏低”、“无影响”。)
)欲测定溶液A中Fe2+的浓度,需要用容量瓶配制某标准溶液,定容时俯视容量瓶的刻度线,会使配制的浓度 。(填“偏高”、“偏低”、“无影响”。)