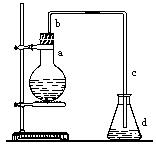
苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应和水解反应的原理,可以进行苯甲酸甲酯的合成和皂化反应。有关物质的物理性质见下表所示:
| | 苯甲酸 | 甲醇 | 苯甲酸甲酯 |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
相关的实验步骤为:
第一步:将过量的甲醇和苯甲酸混合加热发生酯化反应
第二步:水洗提纯
第三步:蒸馏提纯
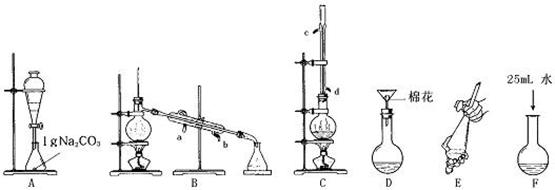
|
(2)C装置中除了装有15g苯甲酸和20mL过量的甲醇外还需要 , ___ 。
(3)C装置中冷凝管的作用是 ,A装置中固体Na2CO3作用是 。
Ⅱ.苯甲酸甲酯的皂化反应
 G H I
G H I(4)能说明G装置中反应完全的现象是 。
(5)在Ⅱ中得到白色固体的质量为5g。假设反应I和反应Ⅱ中:蒸馏提纯的效率为66.7%,加浓盐酸苯甲酸钠生成白色固体的转化率为80%,酯化反应中苯甲酸的转化率为X。其他步骤的转化效率为100%。则X== 。
科学研究发现纳米级的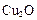 可作为太阳光分解水的催化剂。
可作为太阳光分解水的催化剂。
Ⅰ.四种制取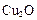 的方法
的方法
(1)火法还原。用炭粉在高温条件下还原CuO;
(2)用葡萄糖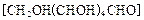 还原新制的
还原新制的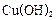 。写出化学方程式 ;
。写出化学方程式 ;
(3)电解法。反应为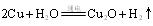 。则阳极产物是 ;
。则阳极产物是 ;
(4)最新实验研究用肼(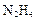 )还原新制
)还原新制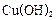 可制备纳米级
可制备纳米级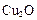 ,同时放出
,同时放出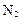 。该制法的化学方程式为 。
。该制法的化学方程式为 。
Ⅱ.用制得的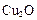 进行催化分解水的实验
进行催化分解水的实验
(1)一定温度下,在2L密闭容器中加入纳米级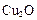 并通入0.10mol水蒸气,发生反应:
并通入0.10mol水蒸气,发生反应: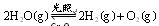 ;△H= +484kJ/mol,不同时段产生
;△H= +484kJ/mol,不同时段产生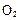 的量见下表:
的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
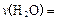 ;达平衡时,至少需要吸收的光能为 kJ。
;达平衡时,至少需要吸收的光能为 kJ。(2)用以上四种方法制得的
 在某相同条件下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。
在某相同条件下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是 。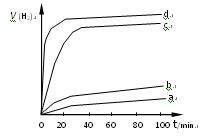
A.c、d方法制得的 催化效率相对较高 催化效率相对较高 |
B.d方法制得的 作催化剂时,水的平衡转化率最高 作催化剂时,水的平衡转化率最高 |
C.催化效果与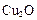 颗粒的粗细、表面活性等有关 颗粒的粗细、表面活性等有关 |
| D.Cu2O催化水分解时,需要适宜的温度 |
(1)以黄铜矿冶炼金属铜的过程中发生反应:2Cu2O+Cu2S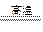 6Cu+SO2↑,反应的氧化剂是_____________________。
6Cu+SO2↑,反应的氧化剂是_____________________。
(2) 黄铜矿熔炼后得到的粗铜含少量Fe、Zn、Ag、Au等金属杂质,需进一步采用电解法精制。在电解精炼铜时,电解液中除了硫酸铜外,往往再加入一些硫酸,其作用是_____________________。
(3)在精炼铜的过程中,电解液中c(Cu2+)逐渐下降,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。下表为几种物质的溶度积。
| 物质 | 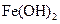 | 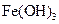 | 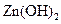 | 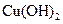 |
溶度积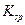 | 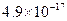 | 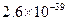 | 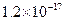 | 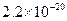 |
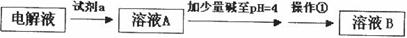
试剂a是__________,其目的是____________________________________;根据溶度积该方案能够除去的杂质金属阳离子是______。操作①用到的玻璃仪器是____________。
(4)工业上通常用FeS除去废水中的Cu2+,写出该沉淀转化离子方程式
I.下列实验操作、试剂保存方法和实验室事故处理,一定正确的是 (填序号)。
| A.实验室中,浓硝酸保存在带橡胶塞的棕色细口试剂并中; |
| B.制备氢氧化铁胶体时,应向20mL沸水中逐滴滴加1~2mL饱和的FeCl3溶液,并继续加热到液体呈透明的红褐色为止; |
C.在石油的分馏实验中,温度 计需插入液体中; 计需插入液体中; |
| D.不慎将浓碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液; |
F.在进行中和热测定时,为保证实验的准确性,我们可以采取以下具体措施:使用碎泡沫以起到隔热保温的作用、使用铜质搅拌棒进行搅拌、取用的碱溶液略过量、进行两到三次实验取平均值。
II.汽车尾气的主要成分为CO2及CO、NOX(NO和NO2)的混合物,其中NO的体积分数占95%以上)等。治理方法之一是在汽车排气管上加装“催化转换器”,利用催化剂使CO和NOX发生反应大部分转化为CO2和N2。某小组在实验室利用下图所示装置模拟处理汽车尾气中CO和NOX的反应并测量反应后混合气体的组成。(已知
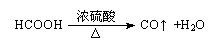 )
)
试回答下列问题:
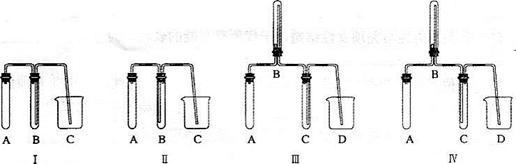
(1)仪器的连接顺序为
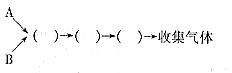
(2)E装置的作用是___________________、___________________________________________。
(3)写出D中的NOX与CO反应的化学方程式______________________________________。
(4)若B容器中生成的NOX为NO,写出该反应的化学方程式,并标出电子转移的方向和数目_____________________________
 ____________________________。
____________________________。(5)若通入的NOX为NO,C装置增重8.8g,收集到的气体在标准状况下为4.48L(其相对分子质量为28.4)。则收集到的气体中NO的物质的量为___________________。
(6)选择高效催化剂,将汽车尾气转化为无毒气体,便彻底解决了汽车尾气对环境的影响,这种说法是否正确并阐述理由:___________________________________________。
(14分)某化学课外兴趣小组为探究苯与液溴之间的反应,进行实验(装置如下图所示)。请根据要求回答相关问题。(已知苯的沸点为80.1 ℃,密度为0.9 g/mL )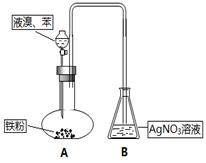
(1)写出苯与液溴反应的化学方程式 反应类型为___________。
(2)锥形瓶中有淡黄色浑浊生成,该组同学经过讨论后认为,依据该现象不能确定发生了以上反应,理由是: ,因此有必要对实验进行改进。
(3)请依据下面的实验流程图选取合适的装置和试剂对上述实验进行改进: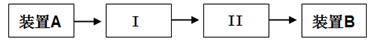
I ________________ , II ___________________
| A.装有NaOH溶液的洗气瓶 | B.装有CC14的洗气瓶 |
| C.装有KI溶液的洗气瓶 | D.装有湿润淀粉KI试纸的集气瓶 |
 以上步骤中:验证沉淀已洗涤干净的方法是_______________________________________。
以上步骤中:验证沉淀已洗涤干净的方法是_______________________________________。②若实验中取用的苯为17.3 mL,液溴为足量,最终测得的沉淀质量为18.8 g,则苯在该反应中的转化率为 ________________,该组同学认为转化率过低,除了可能发生副反应和反应可能进行不完全外,你分析还可能的原因是______________________________________,___________________________________________(请答出2条)
 1)下图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。
1)下图是用KMnO4与浓盐酸反应制取适量氯气的简易装置。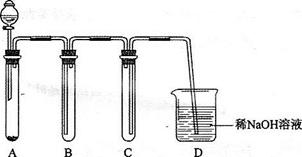
 NH4ClO4 (aq)+NaCl(aq)
NH4ClO4 (aq)+NaCl(aq)

 H2SO4 溶解于锥形瓶中。
H2SO4 溶解于锥形瓶中。 L
L NaOH 溶液。
NaOH 溶液。 NaOH标准溶液滴定至终点,消耗NaOH标准溶液
NaOH标准溶液滴定至终点,消耗NaOH标准溶液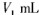
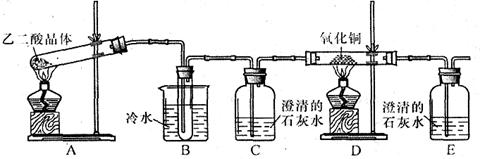
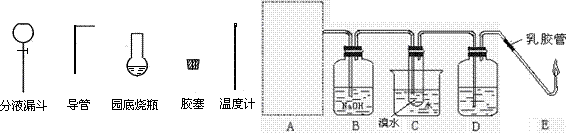
 器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。
器示意图在方框内画出乙烯的发生装置(夹持装置不必画出,需要加热的仪器下方用△标出)。 会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
会产生黑烟,实验时若要迅速熄灭火焰,最简单、安全的操作方法是: 。
 出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)
出实验室制乙酸乙酯的化学方程式(要标出氧-18示踪原子)