(13分)实验室用Na2CO3·10H2O晶体配制240mL 0.1mol/L Na2CO3溶液,回答下列问题:
(1)用托盘天平称取Na2CO3·10H2O的质量为 g。
(2)操作中所需仪器除托盘天平、烧杯、玻璃棒外,还需要 (填仪器名称)。
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次) ;
| A.用蒸馏水洗涤烧杯及玻璃棒2-3次,洗涤液均注入容量瓶,振荡 |
| B.用托盘天平称量所需的Na2CO3·10H2O晶体,放入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其完全溶解 |
| C.将已冷却的Na2CO3溶液沿玻璃棒注入容量瓶中 |
| D.将容量瓶盖紧,振荡摇匀 |
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(4)溶液注入容量瓶前需恢复到室温,这是因为 ;
(5)若出现如下情况,对所配溶液的浓度将有何影响(填“偏高”、“偏低”或“无影响”):
①没有进行A操作 ;
② 称量时,Na2CO3·10H2O已失去部分结晶水 ;
③ 若定容时俯视刻度线 ;
④ 定容摇匀时,发现液面下降,又加水至刻度线 ;
⑤ 容量瓶用蒸馏水洗净后没有干燥 。
配制500mL0.1mol/L碳酸钠溶液。
(1)应用托盘天平称取碳酸钠固体(Na2CO3) g。(4分)
(2)配制碳酸钠溶液时需用到的仪器有 。(4分)
(3)下列操作使溶液物质的量浓度偏低的是: (4分)
| A.没有将洗涤液转移到容量瓶中 |
| B.容量瓶洗净后没经干燥处理 |
| C.转移过程中有少量溶液溅出 |
| D.加水时,水的量超过了刻度线 |
(14分)欲用36.5%(密度为1.18g/cm3)的浓盐酸配制浓度为1.00mol/L的稀盐酸500mL。

(1)选用的主要玻璃仪器有:① ② ③ ④ ⑤ 。
(2)现有下列配制操作,正确的操作顺序为: (填字母)
| A.用量筒量取浓盐酸; | B.反复颠倒摇匀; | C.用胶头滴管加水至刻度线; |
| D.洗净所用仪器,洗涤液也转入容量瓶;E.稀释浓盐酸;F.溶液冷却后转入容量瓶。 |
如果实验室有10mL、50mL、100mL的量筒,应选用 mL的量筒。量取时发现量筒不干净,用水洗净后直接量取,将使配制的溶液浓度 (填“偏高”、“偏低”或“无影响”)。
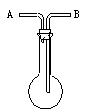

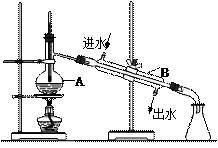
 ,B仪器的名称是 。
,B仪器的名称是 。