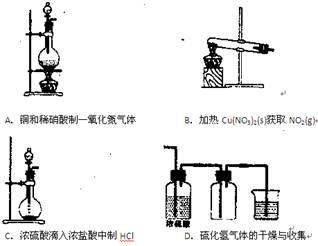
实验室制取干燥的下列气体,收集方法和使用的干燥剂可以完全相同的是
| A.H2和CO2 | B.CO2和O2 | C.Cl2和NH3 | D.NH3和O2 |
下列气体实验室制备时,可以用相同发生装置的是
| A.O2 HCl | B.Cl2 H2 | C.HCl Cl2 | D.CO2 HCl |
下列实验操作中正确的是 ( )
| A.制取溴苯:将铁屑、溴水、苯混合加热 |
| B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 |
| C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 |
| D.检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色 |
如下图所示装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体。该装置可用于( )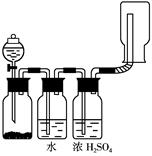
| A.锌和盐酸生成氢气 |
| B.二氧化锰和浓盐酸生成氯气 |
| C.碳酸钙和盐酸生成二氧化碳 |
| D.氯化钠和浓硫酸生成氯化氢 |
某同学用下列装置制备并检验Cl2的性质。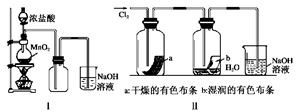
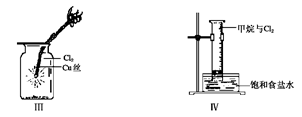
下列说法正确的是( )
| A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗 |
| B.Ⅱ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
| C.Ⅲ图中:生成蓝色的烟 |
| D.Ⅳ图中:量筒中发生了加成反应 |
用98%的浓硫酸(密度为1.84g/cm3 )配制100 mL lmol/L的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒②10 mL量筒③50 mL烧杯④托盘天平⑤100 mL容量瓶⑥胶头滴管⑦玻璃棒,所需仪器按顺序排列正确的是 ( )
| A.④③⑦⑤⑥ | B.②⑤⑦⑥ | C.①③⑤⑥⑦ | D.②⑥③⑦⑤⑥ |
要配制浓度约为2 mol·L-1 NaOH溶液100mL,下面的操作正确的是
| A.称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 |
| B.称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL |
| C.称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| D.用100 mL量筒量取40 mL 5 mol·L-1NaOH溶液,倒入250 mL烧杯中,再用同一量筒取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
根据实验室制取某干燥气体的装置图(如下图所示),判断气体发生装置中的药品可能是( )
| A.FeS和稀H2SO4 |
| B.加热NaCl和浓H2SO4制HCl |
| C.大理石和稀盐酸 |
| D.MnO2和浓盐酸 |
配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是
| A.容量瓶中原有少量的蒸馏水 | B.移液时,不慎将液体流到瓶外 |
| C.容量瓶盛过KOH溶液,使用前未洗涤 | D.定容时俯视刻度线和液面 |