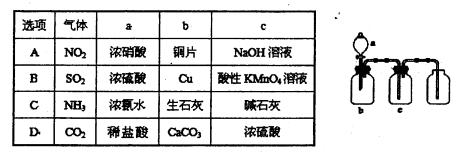
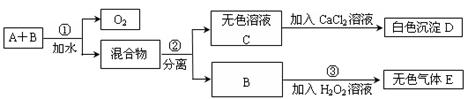
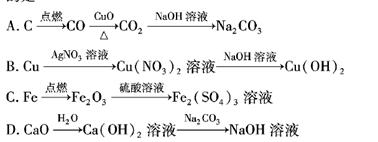
实验室需配制一种强酸溶液500mL,c(H+)=2mol/L,下列配制方法可行的是
A.取100mL5mol/ LH2SO4,加入400mL水 LH2SO4,加入400mL水 |
| B.取200mL5mol/LHCl,加水稀释至500mL |
C.取100 mL 5mol/LH2SO4,加500mL水稀释 5mol/LH2SO4,加500mL水稀释 |
| D.取100 mL5mol/LHNO3,加水稀释至500mL |
下图所示装置是化学实验室的常用装置,它有多种用途.以下各项用途和操作都正确的是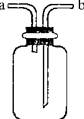
| A.干燥CO2:瓶内放一定体积浓硫酸,由a进气 |
| B.用于收集O2:瓶内充满水,由b进气 |
| C.提供少量CO:瓶内充满CO,b接进水管 |
| D.用做H2S和SO2反应的装置:由a通入H2S,b通入SO2 |
配制一定物质的量浓度的KOH溶液时,导致浓度偏高的原因可能是( )
A.容量瓶中原有少 量的蒸馏水 量的蒸馏水 |
| B.移液时,不慎将液体流到瓶外 |
| C.容量瓶盛过KOH溶液,使用前未洗涤 |
| D.定容时俯视刻度线和液面 |
实验室里需要500mL 0.100mol·L-1的CuSO4溶液,以下配制操作正确的是
A.称取7.68gCuSO4,加入500mL水 | B.称取12.0g胆矾,配成500mL溶液 |
| C.称取8.0gCuSO4,配成500mL溶液 | D.称取8.0g胆矾,配成500mL溶液 |
欲配制100mL 1.0 mol/L Na2SO4溶液,正确的方法是( )
① 将14.2 g Na2SO4 溶于100mL水中;② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL;③ 将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
将14.2 g Na2SO4 溶于100mL水中;② 将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL;③ 将20 mL 5.0 mol/L Na2SO4溶液用水稀释至100 mL
| A.①② | B.②③ | C.①③ | D.①②③ |
(12分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白: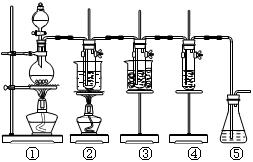
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。
| A.NaBiO3 | B.FeCl3 | C.PbO2 | D.Na2O2 |
 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是① ▲ ; ② ▲ 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 ▲ (填写编号字母);从②的试管中分离出该晶体的方法是 ▲ (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 ▲ 。
为什么? ▲ 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: ▲ 。